题目内容
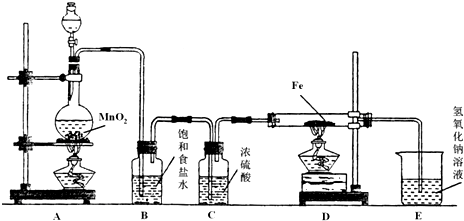
某研究性学习小组设计以图1装置制取氯气,并以氯气为原料进行特定反应.分析并回答下列问题: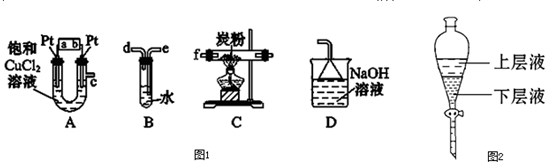
(1)装置A中,b 为电池的
(2)实验开始时,先让氯气和水蒸气充满装有炭粉的装置C,再点燃C处的酒精灯,装置C中发生氧化还原反应,生成CO2和HCl(g),则反应的化学方程式为:
(3)要将装置B接入装置A和C之间,正确的连接顺序是:c→
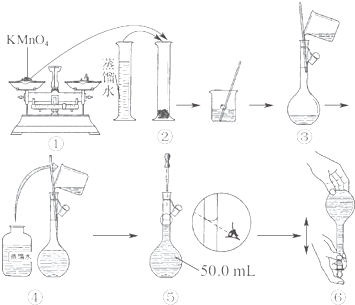
(4)实验结束后,将装置B试管中的氯水倒入已检查完好的分液漏斗中,然后再注入10mL CCl4,盖好玻璃塞,振荡,静置于铁架台上(如图2),等分层后取上层液和下层液,呈黄绿色的是
(5)D装置的作用
分析:(1)电解池中氯离子在阳极失电子生成氯气;
(2)氯气和水蒸气与C反应生成CO2和HCl(g);
(3)氯气通入水中带出水蒸气进入C中与碳反应;
(4)四氯化碳的密度比水大,氯气易溶于有机溶剂;
(5)氯气是有毒的气体,要进行尾气处理;根据电解方程式,结合氯气与氢氧化钠的反应计算.
(2)氯气和水蒸气与C反应生成CO2和HCl(g);
(3)氯气通入水中带出水蒸气进入C中与碳反应;
(4)四氯化碳的密度比水大,氯气易溶于有机溶剂;
(5)氯气是有毒的气体,要进行尾气处理;根据电解方程式,结合氯气与氢氧化钠的反应计算.
解答:解:(1)电解池中氯离子在阳极失电子生成氯气,装置A中c为氯气是出口,所以氯气在与b相连的电极阳极上生成,则b为原电池的正极;
故答案为:正;
(2)在加热条件下,氯气和水蒸气与C反应生成CO2和HCl(g),其反应的方程式为:2Cl2+C+2H2O
4HCl+CO2;
故答案为:2Cl2+C+2H2O
4HCl+CO2;
(3)氯气通入水中带出水蒸气进入C中与碳反应,所以氯气从e进入水,带出水蒸气,从d导管口出来,进入C装置,所以将装置B接入装置A和C之间,正确的连接顺序是:c→e→d→f;
故答案为:e d;
(4)氯水倒入分液漏斗中,然后再注入10mL CCl4,盖好玻璃塞,振荡,静置于铁架台上,由于四氯化碳的密度比水大,四氯化碳在下层,氯气易溶于四氯化碳,所以呈黄绿色的是下层液;
故答案为:下层液;
(5)氯气是有毒的气体,实验中要用氢氧化钠溶液进行尾气处理,防止污染空气;A中的电解方程式为:CuCl2
Cu+Cl2↑,氯气恰好能与100mL 4mol/L的NaOH溶液完全反应,去反应方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,则n(Cl2)=
n(NaOH)=
×0.1L×4mol/L=0.2mol,由电解方程式可知n(Cu)=n(Cl2)=0.2mol,所以m(Cu)=0.2mol×64g/mol=12.8g;
故答案为:吸收尾气,防止污染空气;12.8.
故答案为:正;
(2)在加热条件下,氯气和水蒸气与C反应生成CO2和HCl(g),其反应的方程式为:2Cl2+C+2H2O
| ||
故答案为:2Cl2+C+2H2O
| ||
(3)氯气通入水中带出水蒸气进入C中与碳反应,所以氯气从e进入水,带出水蒸气,从d导管口出来,进入C装置,所以将装置B接入装置A和C之间,正确的连接顺序是:c→e→d→f;
故答案为:e d;
(4)氯水倒入分液漏斗中,然后再注入10mL CCl4,盖好玻璃塞,振荡,静置于铁架台上,由于四氯化碳的密度比水大,四氯化碳在下层,氯气易溶于四氯化碳,所以呈黄绿色的是下层液;
故答案为:下层液;
(5)氯气是有毒的气体,实验中要用氢氧化钠溶液进行尾气处理,防止污染空气;A中的电解方程式为:CuCl2
| ||
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:吸收尾气,防止污染空气;12.8.
点评:本题考查了电解法制备氯气的实验原理、碳与水蒸气氯气的反应、尾气处理等,题目涉及的知识点较多,侧重于考查学生的实验能力和综合应用所学知识解决问题的能力,题目难度中等.

练习册系列答案
相关题目