��Ŀ����
����Ŀ���������۵�ߡ�Ӳ�ȴ������õĿ����Ժ͵��¿���ʴ��.��ҵ���÷�¯��(��Ҫ��FeO��V2O3����������Al2O3��CuO������)��ȡ��������������ͼ��

��֪:
I.���ж��ּ�̬������+5�����ȶ�.������Һ����Ҫ��VO2+��VO3-����ʽ���ڣ�����ƽ�⣺VO2++H2OVO3+2H+.
��.�������ӵij���pH��
Cu2+ | Fe2+ | Fe3+ | |
��ʼ����PH | 5.2 | 7.6 | 2.7 |
��ȫ����PH | 6.4 | 9.6 | 3.7 |
�ش���������
(1)������������ѡ��______________(����ĸ)
a. NaOH��Һ b.��ˮc.������Һ
(2)���յ�Ŀ���ǽ�FeO��V2O3ת��Ϊ������NaVO3��������Ԫ��ȫ��ת��Ϊ+3�۵������д���÷�Ӧ�Ļ�ѧ����ʽ___________________________________
(3)��Һ1����Һ2�Ĺ����У�����pH��8������Ŀ�ģ�һ�dz�ȥ________���ӣ����Ǵ�ʹ_________.
(4)���������еõ�NH4VO3������Ҫϴ�ӣ�д��ʵ����ϴ�ӵIJ�������____________________.
(5)�������ȷ�Ӧ����V2O5ұ������������д����Ӧ�Ļ�ѧ����ʽ____________________________.
(6)���Ļ�����Ҳ�й㷺����;����һ�����������ӿɳ���صĽṹ��ͼ��ʾ.
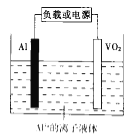
��֪�ŵ�ʱ��ط�ӦΪxAl+VO2=AlxVO2������ŵ�ʱ�����ĵ缫��ӦʽΪ_____________________.
���𰸡�a 4FeO��V2O3+4Na2CO3+5O2![]() 8NaVO3+2Fe2O3+4CO2 Fe3+��Cu2+ VO2+ת��ΪVO3- ϴ��ʱӦ��©����ˮ����û��������ˮ��Ȼ���£��ظ�2
8NaVO3+2Fe2O3+4CO2 Fe3+��Cu2+ VO2+ת��ΪVO3- ϴ��ʱӦ��©����ˮ����û��������ˮ��Ȼ���£��ظ�2![]() 3�� 10Al+3V2O5
3�� 10Al+3V2O5![]() 5Al2O3+6V VO2+xAl3++3xe-=AlxVO2
5Al2O3+6V VO2+xAl3++3xe-=AlxVO2
��������
���ʷ�����ᴿ�ķ����ͻ��������ۺ�Ӧ�á�
������Ҫ����FeO��V2O3��Al2O3��CuO�����м�����������ܽ��γ�ƫ�����Σ����˺���Һ1����ƫ�����Σ�ͨ�������̼�õ����������������������ȷֽ�ɵõ�������������1���������б��գ����������������ܽ⣬��Һ1�к���ͭ���ӡ������ӣ�����pHֵ��8��ͭ���ӡ������ӳ�����ȫ�����˵�����2ӦΪ������ͭ������������ͬʱ������Һ�д���ƽ��VO2++H2OVO3-+2H+������������Ƶ�����NH4VO3������Ҫ������Һ��pHֵ�����˵���Һ2����Ҫ����Ԫ����VO2+��VO3-����ʽ���ڣ��ټ��������ת��ΪNH4VO3�� NH4VO3���յõ�V2O5��V2O5���������ȷ�Ӧ�õ�V���ݴ˽��
������Ҫ����FeO��V2O3��Al2O3��CuO�����м�����������ܽ��γ�ƫ�����Σ����˺���Һ1����ƫ�����Σ�ͨ�������̼�õ����������������������ȷֽ�ɵõ�������������1���������б��գ����������������ܽ⣬��Һ1�к���ͭ���ӡ������ӣ�����pHֵ��8��ͭ���ӡ������ӳ�����ȫ�����˵�����2ӦΪ������ͭ������������ͬʱ������Һ�д���ƽ��VO2++H2OVO3-+2H+������������Ƶ�����NH4VO3������Ҫ������Һ��pHֵ�����˵���Һ2����Ҫ����Ԫ����VO2+��VO3-����ʽ���ڣ��ټ��������ת��ΪNH4VO3�� NH4VO3���յõ�V2O5��V2O5���������ȷ�Ӧ�õ�V��
��1����������ķ�����֪�����Ҫʹ�������ܽ⣬����ֻ����ǿ���ѡa����С���Ϊ��a��
��2�����յ�Ŀ���ǽ�FeO��V2O3ת��Ϊ������NaVO3��������Ԫ��ȫ��ת��Ϊ+3�۵���������ݴ���Ϣ��֪����ʽΪ4FeO��V2O3+4Na2CO3+5O2![]() 8NaVO3+2Fe2O3+4CO2����С���Ϊ��4FeO��V2O3+4Na2CO3+5O2
8NaVO3+2Fe2O3+4CO2����С���Ϊ��4FeO��V2O3+4Na2CO3+5O2![]() 8NaVO3+2Fe2O3+4CO2��
8NaVO3+2Fe2O3+4CO2��
��3����Һ1����Һ2�Ĺ����У�����pH��8һ����ʹͭ���ӡ������ӳ�����ȫ������������Һ�д���ƽ��VO2++H2OVO3-+2H+������������Ƶ�����NH4VO3����С���Ϊ��Fe3+��Cu2+��VO2+ת��ΪVO3-��
��4�����������еõ�NH4VO3������Ҫϴ�ӣ�ϴ��ʱӦ��©����ˮ����û��������ˮ��Ȼ���£��ظ�2![]() 3�Ρ���С���Ϊ��ϴ��ʱӦ��©����ˮ����û��������ˮ��Ȼ���£��ظ�2
3�Ρ���С���Ϊ��ϴ��ʱӦ��©����ˮ����û��������ˮ��Ȼ���£��ظ�2![]() 3�Ρ�
3�Ρ�
��5�����ȷ�Ӧ��V2O5ұ���������Ļ�ѧ����ʽΪ10Al+3V2O5![]() 5Al2O3+6V����С���Ϊ��10Al+3V25
5Al2O3+6V����С���Ϊ��10Al+3V25![]() 5Al2O3+6V��
5Al2O3+6V��
��6���õ�صĸ���Ϊ����ʧ���ӷ���������Ӧ���缫��ӦʽΪAl-3e-=Al3+����ص��ܷ�ӦΪxAl+VO2=AlxVO2������������ӦΪ�ܷ�Ӧ��ȥ������Ӧ�������缫��ӦʽΪVO2+xAl3++3xe-=AlxVO2����С���Ϊ��VO2+xAl3++3xe-=AlxVO2��

����Ŀ���������������ܰ뵼�����Ҫԭ�ϡ���ҵ�ϳ���п��ұ���ķ����л����ء���֪ijп������Ҫ��Zn��Si��Pb��Fe��Ga����������øÿ������صĹ����������£�

��֪��������Ԫ�����ڱ���λ�ڵ������ڵڢ�A����ѧ�����������ơ�
��lg2=0.3��lg3=0.48��
�۲������ʵ�Ksp��F����ʾ
���� |
|
|
|
|
Ksp |
|
|
|
|
��1������1����Ҫ�ɷ���_________��д��ѧʽ����
��2������H2O2��Ŀ����(�����ӷ���ʽ��ʾ)___________��
��3����pH��Ŀ����______�����������£�������Һ�и������ӵ�Ũ�Ⱦ�Ϊ0.01 mol/L������Һ��ij������Ũ��С��![]() mol/Lʱ����Ϊ����������ȫ��ȥ����pHӦ���ڵķ�ΧΪ_______��
mol/Lʱ����Ϊ����������ȫ��ȥ����pHӦ���ڵķ�ΧΪ_______��
��4������D������__________���ˡ�ϴ�ӡ����
��5���Ʊ�����������Ga��
�ٵ�ⷨ�Ʊ������ء��ö��Ե缫���![]() ��Һ�����Ƶý����أ�д�������缫��Ӧʽ_________��
��Һ�����Ƶý����أ�д�������缫��Ӧʽ_________��
�ڵ�ⷨ���������أ����غ�Zn��Fe��Cu�����ʣ���֪������:![]()
�����йص�⾫�������ص�˵����ȷ����_______������ĸ��ţ���
A .��⾫����ʱ�������Դ����������
B. ��⾫�������У����������ļ����������������������
C. ����Cu��Fe�����ڵ��۵ײ��γ�������
D. ���ü���ȼ�ϵ�ص�⾫�������أ���������56.0 g������ʱ����ظ���������ı�״���µ�![]() 6.72 L
6.72 L






