题目内容
【题目】桂皮酸是从肉桂皮中分离出的有机酸,广泛应用于精细化工品的生产。桂皮酸的一条成路线如下,部分需要的试剂或条件略去:

已知:

(1)D中官能团名称为___________________,反应IV的反应类型为______________________。
(2)写出反应I的化学方程式__________________________________________
(3)写出桂皮酸的结构简式____________________________________________
(4)为检验D是否已经完全转化为桂皮酸,所用试剂和实验条件是_________________________。
(5)写出同时满足下列三个条件的C的同分异构体的结构简式__________________
①属于芳香族化合物 ②核磁共振氢谱为四组峰 ③能与 NaHCO3溶液反应产生气体
【答案】碳碳双键、醛基 消去反应 ![]() +2Cl2
+2Cl2![]()
![]() +2HCl
+2HCl ![]() 新制的Cu(OH)2悬浊液、加热(或银氨溶液、加热) :
新制的Cu(OH)2悬浊液、加热(或银氨溶液、加热) : 、
、
【解析】
本题为有机推断题。根据B的分子式可知B为卤代烃,B在氢氧化钠、水、加热条件下发生卤代烃的水解生成醇,此醇发生信息提示中的反应生成![]() ,由此醛可逆推醇为
,由此醛可逆推醇为![]() ,B为
,B为![]() ,A为
,A为![]() ,A生成B的反应为取代反应;
,A生成B的反应为取代反应;![]() 与CH3CHO、稀NaOH条件下发生加成反应生成C,C经反应Ⅳ生成D,D的分子式为C9H8O,根据C的结构简式和D的分子式可推知此反应为消去反应,反应条件为氢氧化钠的醇溶液加热,D的结构简式为
与CH3CHO、稀NaOH条件下发生加成反应生成C,C经反应Ⅳ生成D,D的分子式为C9H8O,根据C的结构简式和D的分子式可推知此反应为消去反应,反应条件为氢氧化钠的醇溶液加热,D的结构简式为![]() ,D经反应Ⅴ生成桂皮酸,根据桂皮酸的分子式可推知此反应Ⅴ为氧化反应,桂皮酸的结构简式为
,D经反应Ⅴ生成桂皮酸,根据桂皮酸的分子式可推知此反应Ⅴ为氧化反应,桂皮酸的结构简式为![]() ,据此解答。
,据此解答。
根据B的分子式可知B为卤代烃,B在氢氧化钠、水、加热条件下发生卤代烃的水解生成醇,此醇发生信息提示中的反应生成![]() ,由此醛可逆推醇为
,由此醛可逆推醇为![]() ,B为
,B为![]() ,A为
,A为![]() ,A生成B的反应为取代反应;
,A生成B的反应为取代反应;![]() 与CH3CHO、稀NaOH条件下发生加成反应生成C,C经反应Ⅳ生成D,D的分子式为C9H8O,根据C的结构简式和D的分子式可推知此反应为消去反应,反应条件为氢氧化钠的醇溶液加热,D的结构简式为
与CH3CHO、稀NaOH条件下发生加成反应生成C,C经反应Ⅳ生成D,D的分子式为C9H8O,根据C的结构简式和D的分子式可推知此反应为消去反应,反应条件为氢氧化钠的醇溶液加热,D的结构简式为![]() ,D经反应Ⅴ生成桂皮酸,根据桂皮酸的分子式可推知此反应Ⅴ为氧化反应,桂皮酸的结构简式为
,D经反应Ⅴ生成桂皮酸,根据桂皮酸的分子式可推知此反应Ⅴ为氧化反应,桂皮酸的结构简式为![]() ;
;
(1)根据上述分析D的结构简式为![]()
(2)根据上述分析A为![]() ,A与氯气、光照生成B,B为
,A与氯气、光照生成B,B为![]() ,此反应为取代反应,方程式为
,此反应为取代反应,方程式为![]() +2Cl2
+2Cl2![]()
![]() +2HCl。本小题答案为:
+2HCl。本小题答案为:![]() +2Cl2
+2Cl2![]()
![]() +2HCl。
+2HCl。
(3)根据上述分析可知桂皮酸的结构简式为![]() 。本小题答案为:
。本小题答案为:![]() 。
。
(4)D为醛,根据醛的特性进行检验,加入新制的氢氧化铜悬浊液、加热会出现砖红色沉淀;或加入银氨溶液、加热有光亮的银析出。本小题答案为:新制的Cu(OH)2悬浊液、加热(或银氨溶液、加热)。
(5)满足下列三个条件的C的同分异构体应为:①属于芳香族化合物含有一个苯环 ②核磁共振氢谱为四组峰含有4中等效氢③能与 NaHCO3溶液反应产生气体含有一个-COOH,则此同分异构体为 、
、 。本小题答案为:
。本小题答案为: 、
、 。
。

【题目】金属钒熔点高、硬度大,具有良好的可塑性和低温抗腐蚀性.工业常用钒炉渣(主要含FeO·V2O3,还有少量Al2O3、CuO等杂质)提取金属钒,流程如图:

已知:
I.钒有多种价态,其中+5价最稳定.钒在溶液中主要以VO2+和VO3-的形式存在,存在平衡:VO2++H2OVO3+2H+.
Ⅱ.部分离子的沉淀pH:
Cu2+ | Fe2+ | Fe3+ | |
开始沉淀PH | 5.2 | 7.6 | 2.7 |
完全沉淀PH | 6.4 | 9.6 | 3.7 |
回答下列问题
(1)碱浸步骤中最好选用______________(填字母)
a. NaOH溶液 b.氨水c.纯碱溶液
(2)焙烧的目的是将FeO·V2O3转化为可溶性NaVO3,其中铁元素全部转化为+3价的氧化物,写出该反应的化学方程式___________________________________
(3)溶液1到溶液2的过程中,调节pH至8有两个目的,一是除去________离子,二是促使_________.
(4)沉钒过程中得到NH4VO3沉淀需要洗涤,写出实验室洗涤的操作方法____________________.
(5)常用铝热反应法由V2O5冶炼金属钒,请写出反应的化学方程式____________________________.
(6)钒的化合物也有广泛的用途,如一种新型铝离子可充电电池的结构如图所示.
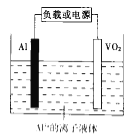
已知放电时电池反应为xAl+VO2=AlxVO2↓,则放电时正极的电极反应式为_____________________.
【题目】已知化学反应①:Fe(s)+CO2(g)![]() FeO(s)+CO(g),其化学平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其化学平衡常数为K1;化学反应②:Fe(s)+H2O(g)![]() FeO(s)+H2(g),其化学平衡常数为K2,在温度973 K和1173 K的情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其化学平衡常数为K2,在温度973 K和1173 K的情况下,K1、K2的值分别如下:
温度 | K1 | K2 |
973 K | 1.47 | 2.38 |
1 173 K | 2.15 | 1.67 |
(1)通过表格中的数值可以推断:反应①是_______(填“吸热”或“放热”)反应。
(2)现有反应③:CO2(g)+H2(g)![]() CO(g)+H2O(g),请你写出该反应的平衡常数K3的表达式:K3=______。
CO(g)+H2O(g),请你写出该反应的平衡常数K3的表达式:K3=______。
(3)根据反应①与②可推导出K1、K2与K3之间的关系式为__________,据此关系式及上表数据,能推断出反应③是________(填“吸热”或“放热”)反应。
(4)要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有______ 、_____ (填写字母序号)。
A.缩小反应容器的容积 B.扩大反应容器的容积
C.升高温度 D.使用合适的催化剂
E.设法减小平衡体系中的CO的浓度
(5)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:

①图甲中t2时刻发生改变的条件是__________。
②图乙中t2时刻发生改变的条件是__________。