题目内容
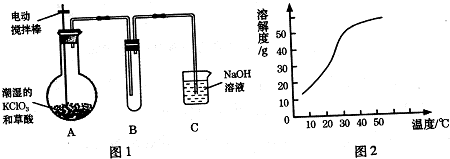
6.下列图象能正确反映对应的实验操作的是( )| A. |  向一定量的饱和石灰水中加入氧化钙 | |
| B. | 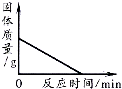 加热一定量高锰酸钾固体产生氧气 | |
| C. | 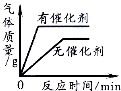 用一定量的双氧水制取氧气 | |
| D. | 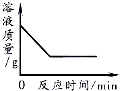 向一定量的硝酸银溶液中插入铜丝 |
分析 A.氧化钙与水的反应生成氢氧化钙,反应为放热反应,氢氧化钙溶解度随着温度升高而降低;
B.加热高锰酸钾的反应生成锰酸钾、二氧化锰和氧气;
C.根据催化剂只能改变化学反应速率,而不影响生成氧气的多少分析解答;
D.铜和硝酸银溶液反应生成银和硝酸铜.
解答 解:A.氧化钙与水的反应生成氢氧化钙,反应为放热反应,氢氧化钙溶解度随着温度升高而降低,故会析出氢氧化钙,溶质质量会变小,然后不变,故A错误;
B.加热高锰酸钾的反应生成锰酸钾、二氧化锰和氧气,高锰酸钾完全反应,剩余固体锰酸钾、二氧化锰,质量不能等于0,故B错误;
C.催化剂只能改变化学反应速率,而不影响生成氧气的多少,所以生成的氧气的质量应该相同,只是有催化剂的放出氧气的速率快,故C错误;
D.铜和硝酸银溶液反应生成银和硝酸铜,所以向一定量的硝酸银溶液中插入铜丝溶液的质量会减少,当反应完毕后溶液质量不变,为一定值,故D正确;
故选:D.
点评 本题考查的是化学实验现象与图象的关系,清楚图象表达的含义,熟悉物质的性质及发生的反应即可解答,题目难度中等.

练习册系列答案
相关题目
16.NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 1.0L 1.0mo1•L-1的NaAlO2水溶液中含有的氧原子数为2NA | |
| B. | 常温常压下,8gO2含有4NA个电子 | |
| C. | 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| D. | 1mol的羟基与1mol的氢氧根离子所含电子数均为9NA |
17.已知A、B、C、D、E是短周期中原子序数依次增大的5种元素,B、C同周期,D、E也同周期,D原子最外层电子数与最内层电子数相等,A、B、C、D的原子序数之和是E的两倍,D单质在C单质中燃烧时剧烈放热并发出耀眼的白光,A、B形成的气态化合物的水溶液呈碱性.下列说法错误的是( )
| A. | 原子半径:D>E>B>C>A | |
| B. | 热稳定性:EA4<A2C | |
| C. | B元素的最高价氧化物的水化物与D单质反应不能生成A2气体 | |
| D. | 化合物DC与化合物EC2中化学键类型相同 |
14.若溶液中加铝可产生H2,则满足此条件的溶液中可能大量存在的离子组是( )
| A. | Al3+Na+HCO3- Cl- | B. | K+ Na+ HCO3-AlO2- | ||
| C. | Mg2+ NH4+ SO42-Cl- | D. | Fe2+ Na+Cl- NO3- |
11.将钠投入到滴有石蕊试液的水中,下列有关现象的叙述中,错误的是( )
| A. | 钠浮在水面上 | B. | 钠熔化成小球并在水面上游动 | ||
| C. | 有无色无味的气体生成 | D. | 水溶液变为红色 |
18.下列物质能够使胃液酸度降低,起到中和过多胃酸作用的是( )
| A. | Na2CO3 | B. | Na2O | C. | CaO | D. | Al(OH)3 |
4.下列各对物质中,互为同系物的是( )
| A. | CH4、C2H4 | B. | CH4、C2H5OH | C. | C2H6、C3H8 | D. | CH3CHO、C3H8 |