题目内容
用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如下图所示,则下列有关说法中正确的是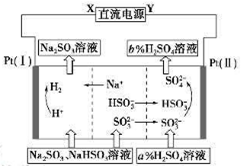
| A.X为直流电源的正极,Y为直流电源的负极 |
| B.阳极区pH减小 |
| C.图中的b<a |
| D.阴极的电极反应为HSO3——2e—+H2O=SO42—+3H+和 SO32——2e—+2H2O=SO42—+4H+ |
B
解析试题分析:因为电解池左室H+→H2,Pt(I)是阴极,X为直流电源的负极,A错误;电解池右室阳极区的发生反应HSO3——2e—+H2O=SO42—+3H+ 和 SO32——2e—+2H2O=SO42—+4H+,故pH减小,B正确;D错误;C.图中的b<a
考点:电解原理。

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
控制适合的条件,将反应2Fe3++2I- 2Fe2++I2设计成下图所示的原电池。下列判断不正确的是
2Fe2++I2设计成下图所示的原电池。下列判断不正确的是

A.为证明反应的发生,可取甲中溶液加入酸性高锰酸钾溶液 |
B.反应开始时,甲中石墨电极上Fe3+被还原,乙中石墨电极上发生氧化反应 |
C.电流计读数为零时,在甲中加入FeCl2固体后,甲中石墨电极为负极 |
| D.此反应正反应方向若为放热反应,电流计读数为零时,降低温度后,乙中石墨电极为负极 |
用惰性电极电解一定量的硫酸铜溶液,实验装置如图1所示。电解过程中的实验数据如图2所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标况)。则下列说法中正确的是

| A.电解过程中,b电极表面先有红色物质析出,然后才有气泡产生 |
| B.从开始到Q点时收集到的混合气体的平均相对分子质量为17 |
| C.曲线OP 段表示H2和O2混合气体的体积变化,曲线PQ段表示O2的体积变化 |
| D.a电极上发生反应的方程式为:2H+ + 2e- = H2↑和4OH-–4 e-=2H2O+ O2↑ |
关于下列各图的说法中,正确的是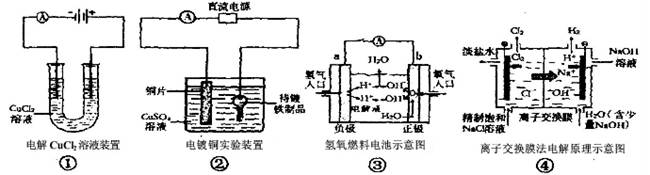
| A.①中与电源负极相连的电极附近能产生使湿润淀粉KI试纸变蓝的气体 |
| B.②中待镀铁制品应该与电源的正极相连接 |
| C.③中的b极是电子流出的极,发生氧化反应 |
| D.④中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 |
下列有关原电池的说法中,正确的是( )
| A.铝片和镁片用导线连接后插入NaOH溶液中,镁片较活泼,作负极 |
| B.铝片和铜片用导线连接后插入浓硝酸中,铜作负极 |
| C.镀锌铁和镀锡铁的镀层破损后,前者较易被腐蚀 |
| D.将反应2Fe3++Fe=3Fe2+设计为原电池,则可用锌片作负极,铁片作正极,FeCl3溶液作电解质 |
关于原电池的叙述正确的是( )
| A.构成原电池的正极和负极必须是两种不同金属 |
| B.原电池是把化学能转变为电能的装置 |
| C.在铅、银和盐酸构成的原电池工作时,铅板上有5.18 g铅溶解,正极上就有1 120 mL(标准状况)气体析出 |
| D.原电池工作时,正极和负极上发生的都是氧化还原反应 |
将纯锌片和纯铜片按下图所示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是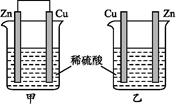
| A.两烧杯中铜片表面均无气泡产生 | B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的酸性均减弱 | D.产生气泡的速率甲比乙慢 |
500 mL NaNO3和Cu(NO3)2的混合溶液中c(NO3- )=0.3 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到气体1.12 L(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是
| A.原混合溶液中c(Na+)=0.2 mol·L-1 |
| B.电解后溶液中c(H+)=0.2 mol·L-1 |
| C.上述电解过程中共转移0.4 mol电子 |
| D.电解后得到的Cu的物质的量为0.1 mol |