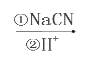题目内容
【题目】某课外活动小组为了检验浓硫酸与木炭在加热条件下反应产生的SO2和CO2气体,设计了如图所示实验装置,a、b、c为止水夹,B是用于储气的气囊,D中放有用I2和淀粉的蓝色溶液浸湿的脱脂棉。
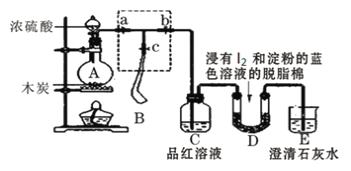
(1)装置A中盛放浓硫酸的仪器名称______________。
(2)装置A中发生反应的化学方程式为___________________________________。
(3)实验时,装置C中的现象为_______________________________________。
(4)此实验成败的关键在于控制反应产生气体的速率不能过快,因此设计了虚框部分的装置,则正确的操作顺序是_________________(用操作编号填写)。
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
③打开止水夹a和c,关闭止水夹b;
(5)当D中产生_________________现象时,可以说明使E中澄清石灰水变浑浊的是CO2,而不是SO2;写出D中发生反应的化学方程式_______________________________________,当D中反应发生0.3mol电子转移时,发生反应的气体的体积(标准状况)是_____________L。
【答案】
(1)分液漏斗 (2分)
(2)C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O (2分,反应物和生成物的化学式全部正确得1分,其它条件、配平等正确得1分)
CO2↑+2SO2↑+2H2O (2分,反应物和生成物的化学式全部正确得1分,其它条件、配平等正确得1分)
(3)品红溶液褪色 (2分)
(4)③①② (2分)
(5)进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变(2分)
I2+SO2+2H2O=2HI+H2SO4(2分,反应物和生成物的化学式全部正确得1分,其它条件、配平等正确得1分) 3.36(2分)
【解析】
试题分析:(1)装置A中盛放浓硫酸的仪器名称为分液漏斗。(2)装置A中浓硫酸有强氧化性,能将C氧化为二氧化碳;D中碘单质能将二氧化硫氧化为硫酸,故答案为:C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O 。(3)反应产生的二氧化硫能使品红溶液褪色。(4)先使气体充满B,用B中气体进行试验,所以操作顺序为:③①②。(5)进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变时出气口出的是二氧化碳,所以现象为:进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变。D中二氧化硫和碘单质反应方程式为:I2+SO2+2H2O=2HI+H2SO4 。反应中1摩尔二氧化硫反应转移2摩尔电子,所以当有0.3摩尔电子转移时,有0.15摩尔的二氧化硫反应,标况下的体积为3.36L。
CO2↑+2SO2↑+2H2O 。(3)反应产生的二氧化硫能使品红溶液褪色。(4)先使气体充满B,用B中气体进行试验,所以操作顺序为:③①②。(5)进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变时出气口出的是二氧化碳,所以现象为:进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变。D中二氧化硫和碘单质反应方程式为:I2+SO2+2H2O=2HI+H2SO4 。反应中1摩尔二氧化硫反应转移2摩尔电子,所以当有0.3摩尔电子转移时,有0.15摩尔的二氧化硫反应,标况下的体积为3.36L。

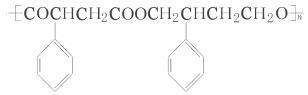
【题目】以下为三种有机物的有关信息,根据表中信息回答问题.
A | B | C |
其产量用来衡量一个国家的石油化工水平. | 比例模型为:
| 沼气主要成分 |
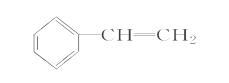
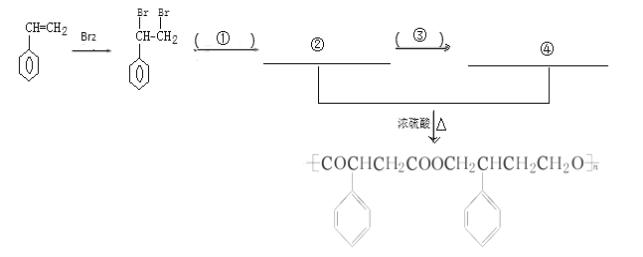
(1)A结构简式是_____________。该物质能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色。其中,与高锰酸钾溶发生的反应是_______________(填反应类型);与溴反应的化学方程式为_____________,当溴的四氯化碳溶液质量增加2.8g时,生成物的质量为__________。
(2)工业上,B来源于煤干馏后的液态产物煤焦油.B与浓硝酸发生取代反应,该反应的化学方程式为__________。
(3)C与氯气反应能生成二氯代物,请写出该反应的化学方程式为__________。
【题目】甲、乙、丙、丁的相互转化关系如图所示(部分反应物及反应条件已略去,箭头表示一步转化)。下列各组物质中,不能满足图示转化关系的是
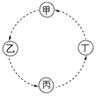
选项 | 甲 | 乙 | 丙 | 丁 |
A |
| CH2=CH2 | CH2BrCH2Br | CH2OHCH2OH |
B | NaAlO2 | Al(OH)3 | Al2O3 | Al |
C | CH3CH2OH | CH3CHO | CH3COOH | CH3COOC2H5 |
D | SiO2 | H2SiO3 | Na2SiO3 | Si |
【题目】用菱锰矿(主要含MnCO3、FeCO3、Al2O3、SiO2)制备MnSO4·H2O的工艺流程如下:
Ⅰ.向菱锰矿中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量MnO2,过滤;
Ⅲ.调节滤液pH=a,过滤;
Ⅳ.浓缩、结晶、分离、干燥得到产品;
Ⅴ.检验产品纯度。
(1)步骤Ⅰ中,滤渣的主要成分是 。
(2)将MnO2氧化Fe2+的离子方程式补充完整:
![]() MnO2 +
MnO2 +![]() Fe2++
Fe2++![]() =
=![]() Mn2+ +
Mn2+ + ![]() Fe3+ +
Fe3+ +![]()
(3)与选用Cl2作为氧化剂相比,MnO2的优势主要在于:原料来源广、成本低、可避免环境污染、 。
(4)已知:生成氢氧化物沉淀的pH
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | |
开始沉淀时 | 3.4 | 6.3 | 1.5 | 7.6 |
完全沉淀时 | 4.7 | 8.3 | 2.8 | 10.2 |
注:金属离子的起始浓度为0.1mol/L
步骤Ⅲ中a的取值范围是 。
(5)步骤Ⅴ,通过测定产品中锰元素的质量分数来判断产品纯度。
已知一定条件下,MnO4-与Mn2+反应生成MnO2 。取x g产品配成溶液,用0.1mol/L KMnO4溶液滴定,消耗KMnO4溶液y mL,产品中锰元素的质量分数为 。
【题目】科学研究与工业生产中常常用到溶液中的反应。
(1)25℃时,0.05 mol·L-1Ba(OH)2溶液的pH= ,将该Ba(OH)2溶液与pH=2的HCl溶液混合,若所得混合溶液pH=7,则Ba(OH)2溶液与HCl溶液的体积比为 。
(2)CO2可转化成有机物实现碳循环:CO2![]() CH3OH
CH3OH![]() HCOOH……
HCOOH……
25 ℃时,几种酸的电离平衡常数如下:
化学式 | HCOOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-4 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
回答下列问题:
①用离子方程式表示HCOONa溶液呈碱性的原因 。
②物质的量浓度均为0.1 mol·L-1的下列四种物质:
a.Na2CO3 b.NaClO c.HCOONa d.NaHCO3 ,pH由大到小的顺序是 (填编号)。
(3)常温下,将0.2 mol·L-1的HCOOH和0.1 mol·L-1的NaOH溶液等体积混合,所得溶液的pH<7,说明所得混合溶液中HCOOH的电离程度 HCOONa的水解程度(填“大于”“等于”或“小于”)。
(4)含有Cr2O72-的废水毒性较大,某工厂废水中含5.00×10-3 mol·L-1的Cr2O72-。为使废水能达标排放,做如下处理:Cr2O72-![]() Cr3+、Fe3+
Cr3+、Fe3+![]() Cr(OH)3、Fe(OH)3。若处理后的废水中残留的c(Fe3+)=2×10-13 mol·L-1,则残留的Cr3+的浓度为 mol·L-1 (已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)。
Cr(OH)3、Fe(OH)3。若处理后的废水中残留的c(Fe3+)=2×10-13 mol·L-1,则残留的Cr3+的浓度为 mol·L-1 (已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)。