题目内容
18.CH4是天然气、沼气的主要成分,目前世界20%的能源需求由它提供.(1)写出CH4的结构式
 .
.(2)CH4是重要的化工原料,可以制备重要溶剂四氯化碳,写出由CH4直接生成四氯化碳的化学方程式CH4+4Cl2$\stackrel{光照}{→}$CCl4+4HCl.
(3)在碳原子数小于10的CH4的同系物中,写出一氯取代物只有一种的烷烃的结构简式:CH3CH3、C(CH3)4(或C(CH3)3C(CH3)3)(任写两种).
分析 (1)根据结构式可以在一定程度上反映真正的分子结构和性质,甲烷分子中1个碳原子和4个氢原子分别形成1个碳氢共价键;
(2)根据取代反应原理写出甲烷与氯气反应生成四氯化碳的方程式;
(3)甲烷的同系物中,一氯取代物只有一种,说明该烷烃中只有一种等效氢原子,根据等效氢原子的判断方法来解答.
解答 解:(1)甲烷是碳原子和氢原子间通过共价单键形成的空间正四面体结构,其结构式为 ,故答案为:
,故答案为: ;
;
(2)1mol甲烷与4mol氯气发生取代反应生成四氯化碳和氯化氢,反应的化学方程式为CH4+4Cl2$\stackrel{光照}{→}$CCl4+4HCl,故答案为:CH4+4Cl2$\stackrel{光照}{→}$CCl4+4HCl;
(3)烷烃分子中,同一个碳上的氢原子等效,连在同一个碳原子上的氢原子等效,具有镜面对称的碳原子上的氢原子等效,烷烃的一氯取代物只有一种,说明该烷烃中只有一种等效氢原子,在碳原子数小于10的所有烷烃的同分异构体中,其一氯取代物只有一种的甲烷的同系物的结构简式为:CH3CH3、C(CH3)4和C(CH3)3C(CH3)3,
故答案为:CH3CH3、C(CH3)4(或C(CH3)3C(CH3)3).
点评 本题考查了甲烷的结构与性质、同分异构体的书写,题目难度中等,注意掌握甲烷的结构与性质,明确同分异构体的概念及书写原则,(3)为难点,需要明确等效H原子的含义及应用方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.两种元素X、Y,其原子核外电子层数分别为a、b,最外层电子数分别为m、n.下列说法不正确的是( )
| A. | 若a<b<m=n=4,则晶体类型相同时,其单质熔点:Y>X | |
| B. | 若8>m>3,则X必定为主族元素 | |
| C. | 若Y的气态氢化物化学式为YHn,且b<4,则该氢化物为非极性分子 | |
| D. | 若a=b=3,8>m>n>b,则元素非金属性:X>Y |
9.下列反应中,水作为还原剂的是( )
| A. | Cl2+H2O=HCl+HClO | B. | 2Na2O2+2H2O=4NaOH+O2? | ||
| C. | 2F2+2H2O=4HF+O2? | D. | 2Na+4H2O=2NaOH+H2? |
6.下列装置或操作能达到实验目的(必要的夹持装置及石棉网已省略)的是( )
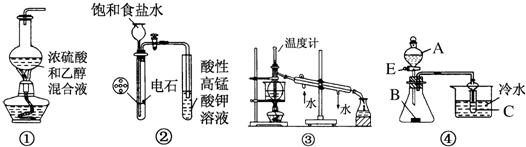

| A. | 图①用于实验室制乙烯 | |
| B. | 图②用于实验室制乙炔并验证乙炔发生氧化反应 | |
| C. | 图③用于实验室中石油的分馏 | |
| D. | 图④中若A为稀硫酸,B为纯碱(固体),C为苯酚钠溶液,则可验证硫酸、碳酸、苯酚酸性的强弱 |
13.将一定体积的NaOH溶液分成两等份,一份用pH=2的一元酸HA溶液中和,消耗酸溶液的体积为V1;另一份用pH=2的一元酸HB溶液中和,消耗酸溶液的体积为V2;则下列叙述正确的是( )
| A. | 若V1>V2,则说明HA的酸性比HB的酸性强 | |
| B. | 若V1>V2,则说明HA的酸性比HB的酸性弱 | |
| C. | 因为两种酸溶液的pH相等,故V1一定等于V2 | |
| D. | HA、HB分别和NaOH中和后,所得的溶液都一定呈中性 |
3.电子构型为[Ar]3d54s2的元素是( )
| A. | ds区元素 | B. | 过渡元素 | C. | 主族元素 | D. | s区元素 |
10.原子序数依次增加的A、B、C、D、E、F六种常见元素中,A、B、C、D是短周期非金属元素,B、C、D同周期,E、F是第四周期的金属元素,F+的三个能层电子全充满.下表是主要化合价及原子半径数据:
请回答下列问题:
(1)B、C、D三种元素第一电离能数值由小到大的顺序是S<P<Cl(填元素符号);
(2)B的氢化物中心原子采取sp3杂化,空间构型是三角锥形,是极性分子(填“极性”或“非极性”);
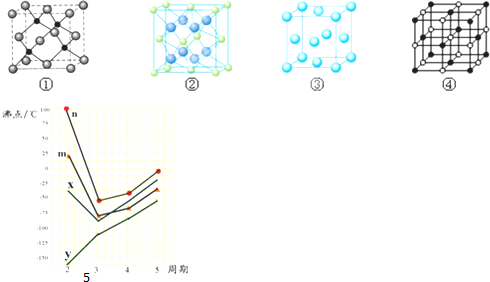
(3)F2+与NH3形成配离子的化学式为[Cu(NH3)4]2+,F单质晶体晶胞是下图的③(填①、②、③或④);
(4)A,E两种元素形成晶体晶胞是图中的②(填①、②、③或④),A离子的配位数是4;若晶胞边长为apm(皮米),则A,E两种粒子的最近距离可表示为$\frac{\sqrt{3}}{4}$apm
(5)图5四条折线分别表示Ⅳ族、VA族、ⅥA族、VⅡA族元素气态氢化物沸点变化,请选出C的氢化物所在的折线n(填n,m,x或y)
| A | B | C | D | E | F | |
| 主要化合价 | -1 | -3+5 | -2+6 | -1+7 | +2 | +1+2 |
| 原子半径nm | 0.071 | 0.11 | 0.102 | 0.099 | 0.197 | 0.117 |
(1)B、C、D三种元素第一电离能数值由小到大的顺序是S<P<Cl(填元素符号);
(2)B的氢化物中心原子采取sp3杂化,空间构型是三角锥形,是极性分子(填“极性”或“非极性”);
(3)F2+与NH3形成配离子的化学式为[Cu(NH3)4]2+,F单质晶体晶胞是下图的③(填①、②、③或④);
(4)A,E两种元素形成晶体晶胞是图中的②(填①、②、③或④),A离子的配位数是4;若晶胞边长为apm(皮米),则A,E两种粒子的最近距离可表示为$\frac{\sqrt{3}}{4}$apm
(5)图5四条折线分别表示Ⅳ族、VA族、ⅥA族、VⅡA族元素气态氢化物沸点变化,请选出C的氢化物所在的折线n(填n,m,x或y)

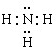 ,B的结构式为
,B的结构式为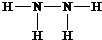 .
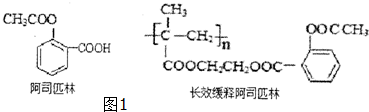
.
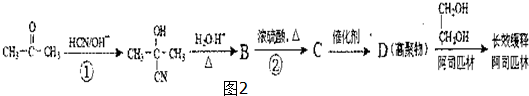
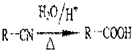 ,回答问题:
,回答问题: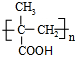 .
.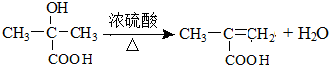 .
.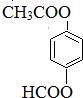 (只写一种).
(只写一种).