题目内容
请写出离子方程式:Fe(NO3)3的酸性溶液中通入足量硫化氢 .
考点:离子方程式的书写
专题:离子反应专题
分析:硫化氢足量,酸性溶液中,氧化性HNO3>Fe3+,则Fe(NO3)3完全反应,以此来解答.
解答:
解:发生氧化还原反应,因硫化氢足量,则Fe(NO3)3完全反应,离子反应为Fe3++3NO3-+2H++5H2S═Fe2++3NO↑+6H2O+5S↓,
故答案为:Fe3++3NO3-+2H++5H2S═Fe2++3NO↑+6H2O+5S↓.
故答案为:Fe3++3NO3-+2H++5H2S═Fe2++3NO↑+6H2O+5S↓.
点评:本题考查离子反应的书写,为高频考点,把握发生的化学反应及电子守恒为解答的关键,侧重氧化还原反应的离子反应考查,题目难度中等.

练习册系列答案
相关题目
可逆反应:2SO2(g)+O2(g)?2SO3(g)在一个体积不变的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内消耗n mol SO2的同时,生成n mol SO2
②单位时间内消耗2n mol SO2的同时,生成n mol O2
③用SO2、O2、SO3的物质的量浓度变化表示的反应速率的比为2:1:2的状态
④混合气体的密度不再改变的状态.
①单位时间内消耗n mol SO2的同时,生成n mol SO2
②单位时间内消耗2n mol SO2的同时,生成n mol O2
③用SO2、O2、SO3的物质的量浓度变化表示的反应速率的比为2:1:2的状态
④混合气体的密度不再改变的状态.
| A、①② | B、①②④ |
| C、①③④ | D、②③④ |
具有相同的质子数和相同电子数的一组微粒是( )
| A、OH-、H2O、F- |
| B、H3O+、NH4+、Na+ |
| C、NH3、NH4+、F- |
| D、Cl-、HS-、S2- |
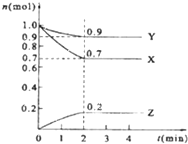 某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示:
某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示:
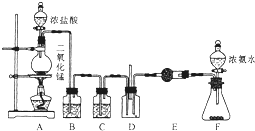 某课外活动小组用如图所示的实验装置探究氯气与氨气之间的反应.其中A、F为氯气和氨气的发生装置,D为纯净、干燥的氯气与氨气反应的装置.
某课外活动小组用如图所示的实验装置探究氯气与氨气之间的反应.其中A、F为氯气和氨气的发生装置,D为纯净、干燥的氯气与氨气反应的装置. Ⅰ.在一定条件下的下列可逆反应达到平衡时,试填出:x A+y B?z C
Ⅰ.在一定条件下的下列可逆反应达到平衡时,试填出:x A+y B?z C