题目内容
可逆反应:2SO2(g)+O2(g)?2SO3(g)在一个体积不变的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内消耗n mol SO2的同时,生成n mol SO2
②单位时间内消耗2n mol SO2的同时,生成n mol O2
③用SO2、O2、SO3的物质的量浓度变化表示的反应速率的比为2:1:2的状态
④混合气体的密度不再改变的状态.
①单位时间内消耗n mol SO2的同时,生成n mol SO2
②单位时间内消耗2n mol SO2的同时,生成n mol O2
③用SO2、O2、SO3的物质的量浓度变化表示的反应速率的比为2:1:2的状态
④混合气体的密度不再改变的状态.
| A、①② | B、①②④ |
| C、①③④ | D、②③④ |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:①单位时间内消耗n mol SO2的同时,生成n mol SO2,正逆反应速率相等,故正确;
②单位时间内消耗2n mol SO2等效于消耗n mol O2,同时生成n mol O2,故正确;
③用SO2、O2、SO3的物质的量浓度变化表示的反应速率的比为2:1:2的状态,一直不变,故错误;
④混合气体的密度不再改变的状态,一直不变,故错误;
所以①②正确,故选A.
②单位时间内消耗2n mol SO2等效于消耗n mol O2,同时生成n mol O2,故正确;
③用SO2、O2、SO3的物质的量浓度变化表示的反应速率的比为2:1:2的状态,一直不变,故错误;
④混合气体的密度不再改变的状态,一直不变,故错误;
所以①②正确,故选A.
点评:本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验设计及其对应的离子方程式均正确的是( )
| A、NaHSO4与NaOH溶液反应:H++OH-=H2O |
| B、少量的Fe与稀硝酸反应:Fe+2H+=Fe2++H2↑ |
| C、实验室利用氢氧化钙固体和氯化铵反应制备氨气:NH4++OH-=NH3↑+H2O |
| D、金属Na与水反应:Na+H2O=Na++OH-+H2↑ |
下列固体投入水中,有气体产生的是( )
| A、Na2CO3 |
| B、Na2O |
| C、NaOH |
| D、Na |
某溶液中含有NH4+、Mg2+、Fe2+、Al3+、SO42-五种离子,若向其中加入过量的氢氧化钡溶液,微热并搅拌,再加入过量的氢碘酸,溶液中大量减少的离子有( )
| A、4 种 |
| B、3 种 |
| C、2 种 |
| D、1 种 |
已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构.下列关于X、Y、Z、W四种元素的描述,正确的是( )
| A、原子半径:X>Y>Z>W |
| B、原子序数:Y>X>W>Z |
| C、原子最外层电子数:Y>X>Z>W |
| D、金属性:X>Y,还原性:W2->Z- |
下列事实不能用勒夏特列原理解释的是( )
| A、打开啤酒瓶盖,瓶口冒出大量气泡 |
| B、合成氨工厂通常采用20MPa~50MPa压强,以提高原料的利用率 |
| C、由H2、I2(g)、HI(g)气体组成的平衡体系减压后颜色变浅 |
| D、工业制取金属钾Na(l)+KCl(l)?NaCl(l)+K(g),选取适宜的温度,使K变成蒸气从反应混合物中分离出来 |
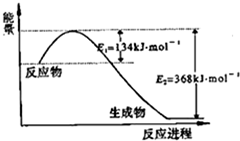 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.