题目内容
具有相同的质子数和相同电子数的一组微粒是( )
| A、OH-、H2O、F- |
| B、H3O+、NH4+、Na+ |
| C、NH3、NH4+、F- |
| D、Cl-、HS-、S2- |
考点:质子数、中子数、核外电子数及其相互联系
专题:原子组成与结构专题
分析:质子数等于各原子的质子数之和,中性微粒中质子数等于电子数,阳离子的电子数等于质子数减去电荷数,而阴离子的电子数为质子数加电荷数.
解答:
解:A、OH-的质子数为8+1=9,电子数为9+1=10,H2O的质子数为8+1×2=10,电子数为10,F-的质子数为9,电子数为9+1=10,故A错误;
B、H3O+的质子数为8+1×3=11,电子数为11-1=10,NH4+的质子数为7+4=11,电子数为11-1=10,Na+的质子数为11,电子数为11-1=10,故B正确;
C、NH3的质子数为7+1×3=10,电子数为10,NH4+的质子数为7+4=11,电子数为11-1=10,F-的质子数为9,电子数为9+1=10,故C错误;
D、Cl质子数为17,电子数为17+1=18,HS-的质子数为1+16=17,电子数为17+1=18,S2-的质子数为16,电子数为16+2=18,故D错误;
故选B.
B、H3O+的质子数为8+1×3=11,电子数为11-1=10,NH4+的质子数为7+4=11,电子数为11-1=10,Na+的质子数为11,电子数为11-1=10,故B正确;
C、NH3的质子数为7+1×3=10,电子数为10,NH4+的质子数为7+4=11,电子数为11-1=10,F-的质子数为9,电子数为9+1=10,故C错误;
D、Cl质子数为17,电子数为17+1=18,HS-的质子数为1+16=17,电子数为17+1=18,S2-的质子数为16,电子数为16+2=18,故D错误;
故选B.
点评:本题考查微粒的质子数和电子数的关系,明确中性微粒、阳离子、阴离子的电子的数目计算是解答的关键,并注意中性微粒中质子数等于电子数.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
有甲、乙、丙、丁四种物质,它们分别是Ba(OH)2、HCl、Na2CO3、Na2SO4中的一种,若将丁的溶液滴入到乙的溶液中,则产生白色沉淀,向这种白色沉淀中滴加甲的溶液,沉淀溶解并放出一种无色气体,据此做出的下列推断中,正确的是( )
| A、甲一定是HCl |
| B、乙一定是Na2CO3 |
| C、丙一定是Na2SO4 |
| D、丁一定是Ba(OH)2 |
对于反应中的能量变化,表述正确的是( )
| A、若反应时形成化学键所释放的能量小于断开旧化学键所吸收的能量则化学反应是吸热反应 |
B、若某化学反应过程中能量变化如图所示,则该化学反应是放热反应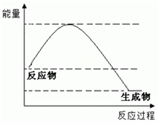 |
| C、化合反应均为放热反应 |
| D、常温下进行的化学反应一定是放热反应,高温下才能发生的反应一定是吸热反应 |
下列说法正确的是( )
| A、碱性:LiOH>NaOH>KOH>RbOH |
| B、金属性:Rb>K>Na>Li |
| C、Rb不易与水反应放出H2 |
| D、和酸反应时Fe能失2个e-,Na失1个e-,所以Fe的金属性强于Na |
下列叙述中正确的是( )
| A、分子组成相差一个或若干个CH2原子团的化合物一定互为同系物 |
| B、苯中加入浓硝酸和浓硫酸的混酸,水浴加热反应,停止反应后,加入氢氧化钠溶液,再用分液漏斗分液,得到粗硝基苯 |
| C、同分异构体由于结构不同,所以化学性质一定不相似 |
| D、在苯中加入溴水,振荡并静置后下层液体为橙黄色 |
下列微粒半径大小比较正确的是( )
| A、Na+<Mg2+<Al3+<F- |
| B、Na<Si<S<Cl |
| C、S2->Cl->Mg2+>Al3+ |
| D、Cs<Rb<K<Na |