题目内容
下列各表述与示意图一致的是
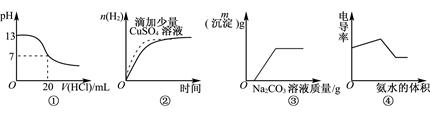

| A.图①表示25℃时,0.1mol·L-1盐酸滴定20mL 0.1mol·L-1NaOH溶液 |
| B.图②表示常温下,等量锌粉与足量的等体积等浓度的盐酸反应 |
| C.图③表示向CaCl2和盐酸的混合溶液中滴加Na2CO3溶液 |
| D.图④表示向盐酸和醋酸混合溶液中滴入氨水 |
C
试题分析:0.1mol?L-1NaOH溶液的pH为13,用0.1mol?L-1盐酸滴定恰好中和时pH为7,因浓度相同,则体积相同,但酸碱中和在接近终点时,pH会发生突变,曲线的斜率会很大,故A错误;图②中锌与硫酸铜反应置换出铜,从而构成铜锌原电池,加快反应速率,但由于消耗了锌生成的氢气减少,B不正确;向CaCl2和盐酸的混合溶液中滴加Na2CO3溶液,碳酸钠首先与盐酸反应,当盐酸被完全消耗后,碳酸钠才能和氯化钙反应生成碳酸钙白色沉淀,C正确;向盐酸和醋酸混合溶液中滴入氨水,生成氯化铵和醋酸铵,溶液的导电性应该是增强的,D不正确,答案选C。
点评:本题结合图象考查了中和滴定、外界条件对反应速率的影响、离子反应以及溶液导电性,属于综合性试题的考查,侧重对学生解题能力的培养,旨在培养学生分析、归纳、总结问题的能力,答题时要做到善于抓规律,有利于调动学生的学习兴趣和学习积极性,也有助于培养学生的逻辑推理能力和抽象思维能力。

练习册系列答案
相关题目
 。
。 K2MnO4+MnO2+ O2↑
K2MnO4+MnO2+ O2↑ 2H2O +O2↑
2H2O +O2↑
 、
、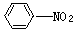 、 己炔、 乙酸四种物质,正确的是
、 己炔、 乙酸四种物质,正确的是