题目内容
下列反应适用于实验室制备氧气的是
①高锰酸钾热分解 2KMnO4 K2MnO4+MnO2+ O2↑
K2MnO4+MnO2+ O2↑
②硝酸铵热分解 2NH4NO3 4H2O+2N2↑+ O2↑
4H2O+2N2↑+ O2↑
③过氧化氢催化分解 2H2O2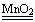 2H2O +O2↑
2H2O +O2↑
④二氧化氮热分解 2NO2 2NO+ O2↑
2NO+ O2↑
①高锰酸钾热分解 2KMnO4
 K2MnO4+MnO2+ O2↑
K2MnO4+MnO2+ O2↑②硝酸铵热分解 2NH4NO3
 4H2O+2N2↑+ O2↑
4H2O+2N2↑+ O2↑③过氧化氢催化分解 2H2O2
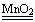 2H2O +O2↑
2H2O +O2↑④二氧化氮热分解 2NO2
 2NO+ O2↑
2NO+ O2↑| A.只有① | B.①和② | C.①和③ | D.①③④ |
C
试题分析:①高锰酸钾热分解气体产物只有氧气,适用于实验室制备氧气;②硝酸铵热分解生成氮气和氧气,不能得到纯净的氧气,不适合;③过氧化氢催化分解产物只有氧气,适用于实验室制备氧气;④二氧化氮热分解生成一氧化氮气体和氧气,二者在常温下又能反应生成二氧化氮气体,得不到氧气,不适合,答案选C。
点评:该题是基础性试题的考查,难度不大。明确实验室制备氧气的原理是答题的关键,有利于培养学生规范、严谨的实验设计能力。注意制备气体时要尽可能的纯净。

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目

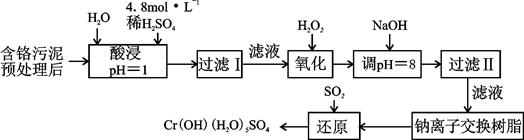
 Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)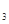 的溶度积Ksp= c(Cr3+)? c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至 。
的溶度积Ksp= c(Cr3+)? c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至 。