题目内容
【题目】海水是重要的资源,可以制备一系列物质。

下列说法正确的是
A. 除去粗盐中 SO42-、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH 溶液→BaCl2 溶液→Na2CO3 溶液→过滤→盐酸
B. 步骤②中,应先通 CO2,再通 NH3
C. 步骤③中可将 MgCl2·6H2O 晶体在空气中直接加热脱水
D. 步骤④、⑤、⑥反应中,溴元素均被氧化
【答案】A
【解析】
A、镁离子用氢氧根离子沉淀,硫酸根离子用钡离子沉淀,钙离子用碳酸根离子沉淀,过滤要放在所有的沉淀操作之后,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子;
B、步骤②是侯德榜制碱的原理,向饱和氯化钠溶液中通入氨气,再通入二氧化碳生成碳酸氢钠晶体;
C、氯化镁水中水解,加热促进水解;
D、步骤④是溴离子被氧化,步骤⑤是溴单质被还原,步骤⑥是溴元素被氧化。
A、镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀,硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,离子都沉淀了,在进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,所以正确的顺序为:加过量的氢氧化钠溶液→加过量的氯化钡溶液→加过量的碳酸钠溶液→过滤→加适量盐酸,故A正确;
B、步骤②中,应先通NH3,再通CO2,目的是增多二氧化碳溶解生成碳酸氢钠晶体,故B错误;
C、步骤③MgCl2·6H2O中氯化镁水解,加热促进水解,晶体不能在空气中直接加热脱水,应在氯化氢气流中加热失水,故C错误;
D、步骤④是溴离子被氧化为溴单质,步骤⑤是溴单质被还原为溴化氢,步骤⑥溴元素被氧化为溴单质,故D错误。
故选A。

 文敬图书课时先锋系列答案
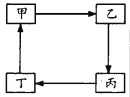
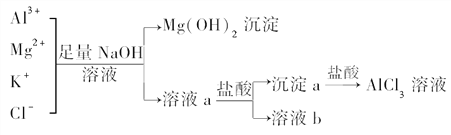
文敬图书课时先锋系列答案【题目】下表所列各组物质中,物质之间不能通过一步反应实现如图转化的是
A | B | C | D |
| |
甲 | Cu | Na2CO3 | Fe | NaAlO2 | |
乙 | CuO | NaOH | FeCl3 | Al2O3 | |
丙 | CuSO4 | NaHCO3 | FeCl2 | AlCl3 | |
丁 | Cu(NO3)2 | CO2 | Fe(NO3)2 | Al(OH)3 |
A. A B. B C. C D. D
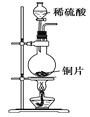
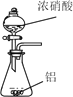
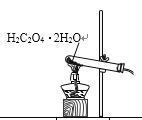
【题目】已知草酸晶体(H2C2O4·2H2O)的熔点为101℃,170℃分解。下列选用的装置和药品能达到实验目的的是
A | B | C | D |
|
|
|
|
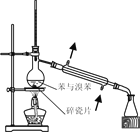
制取SO2 | 制取NO2 | H2C2O4·2H2O分解 | 分离苯与溴苯 |
A. A B. B C. C D. D