题目内容
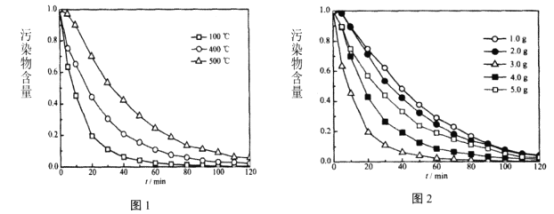
【题目】某溶液中可能含有H+,Na+,![]() ,Mg2+,Fe3+,Al3+,
,Mg2+,Fe3+,Al3+,![]() ,
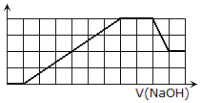
,![]() 等离子.当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图像如图所示,下列说法不正确的是( )
等离子.当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图像如图所示,下列说法不正确的是( )
A.原溶液中含有的阳离子是H+,![]() ,Mg2+,Al3+
,Mg2+,Al3+
B.原溶液中一定含有![]() ,一定不含
,一定不含![]()
C.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
D.反应最后形成的溶液中含有的溶质除了Na2SO4外还有其它物质
【答案】A
【解析】
加入NaOH溶液,开始时没有沉淀生成,说明溶液中含有氢离子;根据产生的沉淀量与加入NaOH的物质的量之间的关系图可知,沉淀部分溶解,则溶液中一定含有Al3+,根据离子共存可知,溶液中一定不存在CO32-;
当沉淀达到最大值时,继续进入氢氧化钠,沉淀不变,这说明溶液中还存在NH4+;根据溶液电中性可知,溶液中还必须存在阴离子,所以一定还有SO42-;
从生成沉淀和溶解沉淀耗碱体积比值可知,若为Fe3+,则Fe3+和Al3+的物质的量之比为1:1,刚好与纵坐标数据吻合;若为Mg2+,Mg2+和Al3+的物质的量之比为1.5:1,不能与纵坐标数据吻合,所以溶液中一定含有Fe3+,一定不含Mg2+。
滴加NaOH溶液未生成沉淀前发生反应:H++OH-=H2O,沉淀达到最大值后继续滴加NaOH溶液发生反应:NH4++OH-=NH3H2O,沉淀溶解时发生反应Al(OH)3+OH-=AlO2-+2H2O,故可以肯定溶液中一定有的离子为:H+、NH4+、Al3+;从ab和cd耗碱体积比值可知,若为Fe3+,则Fe3+和Al3+的物质的量之比为1:1,刚好与纵坐标数据吻合;若为Mg2+,Mg2+和Al3+的物质的量之比为1.5:1,不能与纵坐标数据吻合,所以溶液中一定含有Fe3+,一定不含Mg2+;
A.溶液中含有的阳离子必定有Fe3+、H+、NH4+、Al3+,一定不存在Mg2+,故A错误;
B.由分析知:原溶液中一定含有![]() ,一定不含
,一定不含![]() ,故B正确;
,故B正确;
C.根据分析可知,原溶液中含有的Fe3+和Al3+,且二者的物质的量相等,即其物质的量之比为1:1,故C正确;
D.反应最后形成的溶液中含有的溶质除了Na2SO4外,还含有NaAlO2,故D正确;
故答案为A。

 名校课堂系列答案
名校课堂系列答案