题目内容
【题目】DCCNa (二氯异氰尿酸钠)固体是一种高效、安全的消毒剂。20℃以上易溶于水。(CNO)3H3 (氰尿酸)为三元弱酸。
I.制备DCCA (二氯异氰尿酸)装置如图。主要反应有:
碱溶 (CNO)3H3+ 2NaOH=(CNO)3Na2H + 2H2O △H<0
氯化 (CNO)3Na2H +2Cl2=(CNO)3Cl2H + 2NaCl H<0
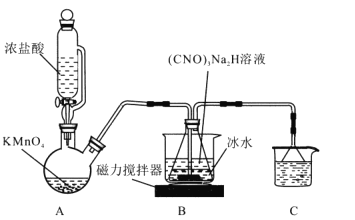
回答下列问题:
(1)装置C中的溶液是______________,作用为______________。
(2)装置A中反应的离子方程式为_______________。
(3)装置B用冰水浴的原因是__________, 碱溶时若氢氧化钠过量,(CNO)3Na2H中可能混有的杂质是__________。
Ⅱ.制备DCCNa
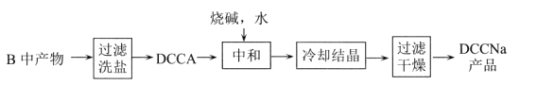
(4)步骤II中过滤洗盐”洗去的盐是__________________。
(5)“中和”反应的化学方程式为_________________。
(6)氧元素含量的测定:称取0. 1000 g DCNa样品,加入一定量醋酸溶液溶解,样品中的氯元素全邵转化成HClO,再加入足量的KI溶液,用淀粉作指示剂, 用01000 mol·L-1Na2S2O3标准溶液滴定生成的碘,消耗VmL.已知: I2+2S2O32-=2I-+S4O62-,样品中氯元素的质量分数=__________%
【答案】氢氧化钠溶液 吸收多余氯气,防止污染空气 ![]() 该反应放热,冰水浴可降温促进反应向正反应方向进行,同时降低产品溶解度 (CNO)3Na3 NaCl
该反应放热,冰水浴可降温促进反应向正反应方向进行,同时降低产品溶解度 (CNO)3Na3 NaCl ![]() 1.775V
1.775V
【解析】
由图中装置和实验药品可知,A装置为氯气发生装置,B装置发生氯化反应生成DCCA,C装置用于尾气处理,吸收多余的氯气。利用DCCA生产DCCNa先将B中产物主要成分为DCCA和NaCl的混合物进行过滤洗盐,得到DCCA,DCCA与氢氧化钠反应得到DCCNa,再经过冷却结晶,过滤干燥得到产品DCCNa,以此分析。
(1)由上述分析可知C装置用于尾气处理,吸收多余的氯气,防止污染空气,试剂为氢氧化钠溶液,故答案为:氢氧化钠溶液;吸收多余氯气,防止污染空气;
(2)A装置为氯气发生装置离子反应为:![]() ,故答案为:
,故答案为:![]() ;
;
(3)由已知反应可知装置B中反应![]() ,该反应放热,冰水浴可降温促进反应向正反应方向进行,同时降低温度可降低产品溶解度;(CNO)3H3 (氰尿酸)为三元弱酸,则碱溶时若氢氧化钠过量,则会生成产物(CNO)3Na3,故答案为:该反应放热,冰水浴可降温促进反应向正反应方向进行,同时降低产品溶解度;(CNO)3Na3;
,该反应放热,冰水浴可降温促进反应向正反应方向进行,同时降低温度可降低产品溶解度;(CNO)3H3 (氰尿酸)为三元弱酸,则碱溶时若氢氧化钠过量,则会生成产物(CNO)3Na3,故答案为:该反应放热,冰水浴可降温促进反应向正反应方向进行,同时降低产品溶解度;(CNO)3Na3;
(4)B中产物主要成分为DCCA和NaCl的混合物,则过滤洗盐洗去的盐是NaCl,故答案为:NaCl;
(5)DCCA与氢氧化钠反应得到DCCNa化学方程式为:![]() ,故答案为:
,故答案为:![]() ;
;
(6)DCCNa样品,加入一定量醋酸溶液溶解,样品中的氯元素全邵转化成HClO,再加入足量的KI溶液,用Na2S2O3标准溶液滴定生成的碘,则关系式为:![]() ,则氯原子的物质的量
,则氯原子的物质的量![]() ,则样品中氯元素的质量分数为
,则样品中氯元素的质量分数为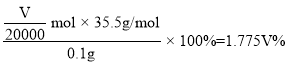 ,故答案为:1.775V。
,故答案为:1.775V。