题目内容
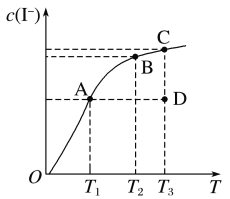
【题目】I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)![]() I3-(aq) ΔH。某I2、KI混合溶液中,I-的物质的量浓度c(I-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是( )
I3-(aq) ΔH。某I2、KI混合溶液中,I-的物质的量浓度c(I-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是( )
A.该反应ΔH>0
B.若反应进行到状态D时,一定有v正>v逆
C.若在T1、T2温度下,反应的平衡常数分别为K1、K2,则K1>K2
D.状态A与状态B相比,状态A的c(I3-)大
【答案】AB
【解析】
A.随着温度升高,碘离子的浓度升高,平衡逆向移动,则证明正反应放热,A项错误;
B.D点要达到平衡状态(C点),碘离子的浓度要升高,即平衡要逆向移动,也就是说逆反应速率大于正反应速率,B项错误;
C.已经分析过正反应放热,则温度越高平衡常数越小,即![]() ,C项正确;
,C项正确;
D.A与B相比反应物更少,则A的生成物更多,D项正确;
故答案选AB。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目