��Ŀ����
����Ŀ��������������{[CH3CH(OH)COO]2Fe��3H2O}(��Է���������288)����������FeCO3��Ӧ�Ƶã���������ˮ�������������Ҵ��������ֽ⣬��һ�ֺܺõIJ�������
I���Ʊ�̼��������װ����ͼ��ʾ��
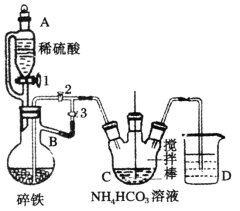
(1)����B��������_________________________��
(2)ʵ��������£��رջ���2������1��3����������ϡ���ᷴӦһ��ʱ�䣬��Ŀ���ǣ�__________��Ȼ��رջ���1���������IJ����ǣ�______��C�з�����Ӧ�����ӷ���ʽΪ_____________��
���Ʊ�����������
����FeCO3�����������������Һ����75���½���ʹ֮��ַ�Ӧ��
(3)�÷�Ӧ��ѧ����ʽΪ______��Ϊ��ֹ�����������ʣ���������ϵ�л�Ӧ����____����Ӧ������������Һ�л��������������ķ����ǣ�_________����ȴ�ᾧ�����ˣ�_________�����
�������������崿�ȵIJ�����
(4)��K2Cr2O7�ζ����ⶨ��Ʒ��Fe2+�ĺ���������Ʒ���ȣ���ȡ6.00g��Ʒ���Ƴ�250��00mL��Һ��ȡ25��00mL��0.0167mol��L-1��K2Cr2O7����Һ�ζ����յ㣬���ı�Һ20��00mL�����Ʒ��������������Ĵ���Ϊ___(������������ʾ)��
���𰸡�������ƿ �ž�װ���ڵĿ�������ֹ������������ �رջ���3������2 Fe2++2HCO3-==FeCO3��+CO2��+H2O 2CH3CH(OH)COOH+FeCO3==[CH3CH(OH)COO]2Fe+CO2��+H2O �������� ������������������ �������Ҵ�ϴ�� 96.2��
��������
(1)��������������;��д����B�����ơ�
(2)��������ϡ���ᷴӦһ��ʱ�䣬�����������ų��������ų������������������뵽����װ������̼�����������Ӧ����̼��������
(3)�����̼��������Ӧ�������������Ͷ�����̼���������۷�ֹ�����������ʣ���Ӧ������Ҫ���������������������������������������Ҵ�������������Ҵ�ϴ�ӡ�
(4)���ݹ�ϵʽ�������������ʵ������ټ��㴿�ȡ�
(1)����B��������������ƿ���ʴ�Ϊ��������ƿ��
(2)ʵ��������£��رջ���2������1��3����������ϡ���ᷴӦһ��ʱ�䣬�����������ų���������Ŀ���ǣ��ž�װ���ڵĿ�������ֹ��������������Ȼ��رջ���1���������IJ����ǣ��رջ���3������2��C�з�����Ӧ�����ӷ���ʽΪFe2++2HCO3��= FeCO3��+CO2��+H2O���ʴ�Ϊ���ž�װ���ڵĿ�������ֹ���������������رջ���3������2��Fe2++2HCO3��= FeCO3��+CO2��+H2O��
(3)�����̼��������Ӧ�������������Ͷ�����̼���䷴Ӧ��ѧ����ʽΪ2CH3CH(OH)COOH + FeCO3==[CH3CH(OH)COO]2Fe+CO2��+H2O��Ϊ��ֹ�����������ʣ���������ϵ�л�Ӧ�������ۣ���Ӧ������������Һ�л�������������壬��Ҫ�����������������������Ҫ�����������������ɣ����˺����������Ҵ�ϴ�ӣ��ʴ�Ϊ��2CH3CH(OH)COOH + FeCO3==[CH3CH(OH)COO]2Fe+CO2��+H2O�������������������ɣ��������Ҵ�ϴ�ӡ�
(4) K2Cr2O7 ���� 6 Fe2+
1mol 6mol
0.0167mol��L-1��0.02L xmol
1mol��0.0167mol��L-1��0.02L = 6mol��xmol
���x = 2.004��10-3mol
![]() ���ʴ�Ϊ96.2%��
���ʴ�Ϊ96.2%��