题目内容
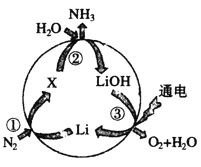
【题目】为体现节能减排的理念,中国研制出了新型固态氧化物燃料电池(SOFC),该电池的工作原理如图所示。下列说法正确的是( )
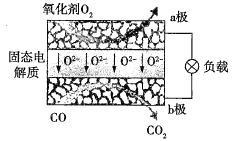
A.可以选用NaOH固体作固态电解质
B.正极的电极反应式为O2+4e-+2H2O=4OH-
C.电子从b极经导线流向a极
D.若反应中转移1 mol电子,则生成22.4 L(标准状况下)CO2
【答案】C
【解析】
该燃料电池中,CO是燃料,所以CO失电子发生氧化反应,则CO所在的b电极为负极,通入氧气的a电极是正极,正极上氧气得电子发生还原反应,电子从负极沿外电路流向正极,据此分析解答。
A.因为NaOH与CO2会发生反应,所以不可以选用NaOH固体作固态电解质,A错误;
B.通入氧气的a电极是正极,正极上氧气得电子发生还原反应,电极反应式为O2+4e-=2O2-,B错误;
C.外电路中,电子从负极b极经导线流向正极a极,C正确;
D.CO所在的b电极为负极,电极反应式为CO-2e-+O2-=CO2,所以反应中转移1 mol电子,则生成0.5 mol CO2,温度压强不知不能计算气体体积,D错误;
故合理选项是C。

练习册系列答案
相关题目
【题目】下列实验中,对应的操作、现象以及所得出的结论都正确的是( )
选项 | 实验 | 现象 | 结论 |
A. | 把铝箔插入浓硝酸中 | 有大量红棕色气体产生 | 浓硝酸具有强氧化性 |
B. |
| 品红褪色 |
|
C. | 淀粉在酸催化水解后的溶液加入新制 | 无砖红色沉淀 | 淀粉水解产物不含葡萄糖 |
D. | 将充满 | 红棕色变深 | 反应 |
A.AB.BC.CD.D