题目内容
【题目】下面是某化学兴趣小组的同学学习元素周期律时设计的两套实验方案。
(实验一)实验步骤如下:
向新制的Na2S溶液中滴加新制的氯水
设计该实验方案的目的是:探究同周期元素的性质递变规律。
(1)实验①的现象是_____________________,反应的离子方程式是_________________。
(实验二)为验证Cl、Br的非金属性强弱,设计了如下实验:(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)实验步骤如图.
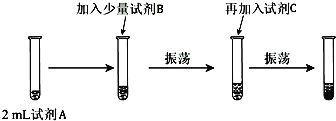
(2)试剂A是NaBr溶液,试剂B是氯水,加C后出现分层,则试剂C是____________.
(3)加入C振荡、静置后看到的现象是:______________________________________。以上反应可以证明Cl的非金属性__________(填“强于”或“弱于”)Br的非金属性。
【答案】有淡黄色沉淀生成 Cl2+S2-=2Cl-+S↓ CCl4 分层,下层紫红色 强于
【解析】
(1)氯水与硫化钠反应生成S与NaCl,S为淡黄色且不溶;【实验二】根据同一氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性来设计实验。
(1)由于氯元素的非金属性强于硫元素,所以Cl2可以置换S,实验①的现象是有淡黄色沉淀生成,反应的离子方程式是Cl2+S2-=2Cl-+S↓;
答案:有淡黄色沉淀生成 Cl2+S2-=2Cl-+S↓
【实验二】
根据同一氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性来设计实验,氯气可以置换溴,再加入萃取剂萃取观察现象;
(2)因为酒精和水任意比互溶,不可做萃取剂;因为四氯化碳与水互不相溶,与溶液互不反应,溴在四氯化碳中的溶解度远远大于在水中的溶解度,所以选择四氯化碳为萃取剂;
答案:CCl4
(3)因为四氯化碳密度比水大,加入四氯化碳振荡、静置后看到的现象是:分层,下层呈紫红色。以上反应可以证明Cl的非金属性强于Br的非金属性;
答案:分层,下层紫红色 强于

 春雨教育同步作文系列答案
春雨教育同步作文系列答案