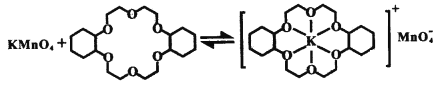
题目内容
【题目】甲醛(![]() )在Ni催化作用下加氢可得甲醇(CH3OH),以下说法中正确的是
)在Ni催化作用下加氢可得甲醇(CH3OH),以下说法中正确的是
A. 甲醛分子间可以形成氢键B. 甲醛分子和甲醇分子内C原子均采取sp2杂化。
C. 甲醛为极性分子D. 甲醇的沸点远低于甲醛的沸点
【答案】C
【解析】
A.甲醛分子中与H形成共价键的C原子的电负性没有那么大,与其相连的H原子不会成为“裸露”质子,甲醛分子间不存在氢键,A项错误;
B.甲醛中C原子形成3个σ键和1个π键,C上没有孤电子对,其中C为sp2杂化,甲醇分子中C原子形成4个σ键,C上没有孤电子对,其中C为sp3杂化,B项错误;
C.甲醛分子为平面三角形,分子中正负电中心不重合,是极性分子,C项正确;
D.甲醇分子中有—OH,可以形成分子间氢键,甲醇的沸点比甲醛的沸点高,D项错误;
本题答案选C。

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
【题目】下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题:
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(1)原子半径最小的元素是___(填元素名称),写出⑥的离子结构示意图___。
(2)③的单质的电子式为__。
(3)以上9种元素中最高价氧化物对应水化物酸性最强的是___(填化学式)。
(4)⑤与⑦形成的化合物中,化学键类型为___。
(5)②与④形成的原子个数比为1:2的化合物的结构式为____。
(6)③、④、⑥的原子半径由大到小的顺序为___(用元素符号回答)。
(7)为探究元素②和⑧的非金属性强弱,某同学设计了如图所示的装置进行实验(夹持仪器已略去,装置气密性良好)。请回答:
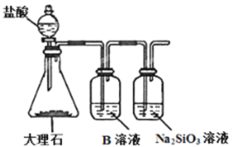
a.溶液B的作用是___。
b.上述实验中,能说明②和⑧非金属性强弱的化学方程式是___。