题目内容
18.下列既能和稀硫酸反应又能和氢氧化钠溶液反应的化合物是( )| A. | 氢氧化铁 | B. | 金属铝 | C. | 氧化铝 | D. | 硫酸铜 |
分析 中学常见的既能与酸反应又能与碱反应的物质主要有:Al、两性氧化物、两性氢氧化物、多元弱酸的酸式盐、弱酸的铵盐、氨基酸、蛋白质等,注意产物为盐与水,注意Al为单质.
解答 解:A.氢氧化铁与硫酸反应生成硫酸铁与水,不能与氢氧化钠溶液反应,故A错误;
B.Al与硫酸酸生成硫酸铝与氢气,与氢氧化钠溶液反应生成偏铝酸钠与氢气,但Al是单质,不属于化合物,故B错误;
C.氧化铝属于两性氧化物,与硫酸反应生成硫酸铝由水,与氢氧化钠溶液反应生成偏铝酸钠与水,故C正确;
D.硫酸铜与氢氧化钠溶液反应生成氢氧化铜与硫酸钠,但不能与硫酸反应,故D错误,
故选:C.
点评 本题考查元素化合物的性质,比较基础,注意基础知识的积累与归纳总结.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
8.某烃的组成中含碳、氢元素的质量比为6:1,该烃对氮气的相对密度为2,该烃能与H2发生加成反应,所得加氢产物的二氯代物有三种同分异构体,则该烃为( )
| A. | CH2=CH-CH2-CH3 | B. | CH2=CH2 | C. | CH3-CH=CH-CH3 | D. | 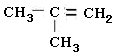 |
13.N20俗称“笑气”,医疗上曾用作可吸入性麻醉剂,下列反应能产生N20:3C0+2N02=3C02+N2O.下列关于N20的说法一定正确的是( )
| A. | 上述反应中,每消耗2mol NO2,就会生成22.4L N20 | |
| B. | N20有氧化性,且为HN02的酸酐 | |
| C. | 等质量的N20和C02含有相等的电子数 | |
| D. | N20会迅速与人体血红蛋白结合,使人中毒 |
7.下列离子方程式正确的是( )
| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+=SO2↑+H2O | |
| B. | CuSO4溶液与过量浓氨水反应的离子方程式:Cu2++2NH3-H2O=Cu(OH)2↓+2NH4+ | |
| C. | 0.01mol/LNH4Al(SO4)2溶液与0.02mol/LBa(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2 H2O | |
| D. | 向CuSO4溶液中加入Na2O2:2 Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑ |
8.下列离子反应方程式正确的是( )
| A. | 向溶Ca(ClO)2液中通入少量SO2:Ca2++3ClO-+SO2 +H2O═CaSO4 ↓+Cl-+2HClO | |
| B. | 1mol/L的NaAlO2 溶液和2.5mol/L的盐酸等体积均匀混合:2AlO2-+5H+═A l(OH)3 ↓+Al3++H2O | |
| C. | 将11.2L标准状况下的氯气通入200mL 2mol/LFeBr2 的溶液中,离子反应方程式为:2Fe2++8Br-+5Cl2 ═2Fe3++4Br2 +10Cl- | |
| D. | 氢氧化亚铁溶于稀硝酸中:Fe(OH)2 +2H+═Fe2++H2O |

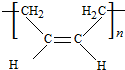
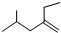 的系统命名4-甲基-2-乙基-1-戊烯.
的系统命名4-甲基-2-乙基-1-戊烯.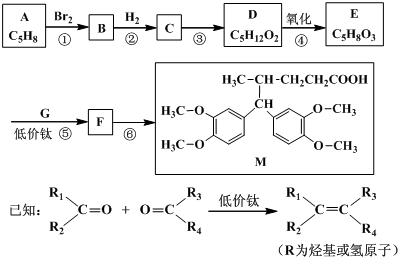
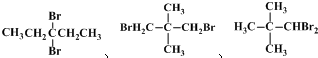 (其中之一);.
(其中之一);.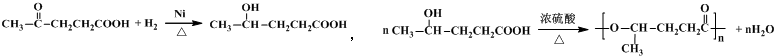 或
或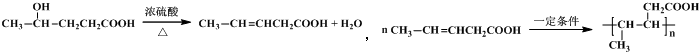 或
或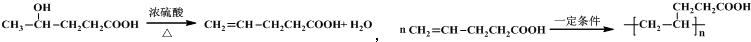 .
.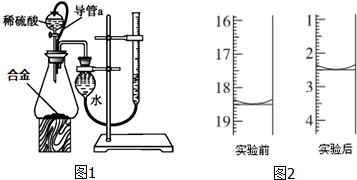 可利用以下方法测定铝镁合金(不含其它元素)组分含量
可利用以下方法测定铝镁合金(不含其它元素)组分含量