题目内容
4.下列除杂操作可行的是( )| A. | 通过浓硫酸除去HCl中的H2O | |
| B. | 通过灼热的镁粉除去N2中的O2 | |
| C. | 制二氧化氮时,用水或NaOH溶液吸收尾气 | |
| D. | 制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体 |
分析 A.浓硫酸具有吸水性,与HCl不反应;
B.二者均与Mg反应;
C.二氧化氮与水反应生成一氧化氮;
D.HCl气体能与碳酸氢钠反应生成CO2,引入新的杂质气体.
解答 解:A.浓硫酸具有吸水性,与HCl不反应,则通过浓硫酸除去HCl中的H2O,操作可行,故A正确;
B.二者均与Mg反应,将原物质反应掉,不符合除杂的原则,则应通过通过灼热的铜网除去N2中的O2,故B错误;
C.二氧化氮与水反应生成一氧化氮,仍然污染空气,所以不能用水吸收,故C错误;
D.实验室制取氯气含有氯化氢和水分,常用饱和食盐水和浓硫酸净化气体,若饱和NaHCO3溶液,HCl会和NaHCO3反应生成CO2,引入新的杂质,故D错误.
故选A.
点评 本题考查物质分离、提纯方法的选择和气体的制备与收集,为高频考点,把握物质的性质及除杂的原则为解答的关键,注意原物质与杂质的性质差异,题目难度不大.

练习册系列答案
相关题目
14.实验室常用反应NaNO2+NH4Cl=NaCl+N2↑+2H2O制取N2.下列有关说法正确的是( )
| A. | NaNO2是氧化剂 | B. | N2的电子式是 | ||
| C. | 生成1 mol N2时转移6 mol 电子 | D. | 氧化剂和还原剂的质量之比是1:1 |
15.下列各组物质中,最简式相同,但既不是同系物,又不是同分异构体的是( )
| A. | 丙烯、环丙烷 | B. | 乙酸、甲酸甲酯 | C. | 乙烯、1-丁烯 | D. | 甲醛、甲酸甲酯 |
12.下列表示对应化学反应的离子方程式正确的是( )
| A. | 用白醋除铁锈:Fe2O3+6H+═3H2O+2Fe3+ | |
| B. | 向NH4HCO3溶液中加入过量的Ba(OH)2溶液并加热:Ba2++2OH-+NH4++HCO3-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+2H2O+BaCO3↓ | |
| C. | AlCl3溶液中滴加浓氨水至过量:Al3++4NH3˙H2O═AlO2-+4NH4++2H2O | |
| D. | MnO2与浓盐酸反应制取Cl2:MnO2+4H++4Cl-═Mn2++2Cl2↑+2H2O |
19.羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸在一定的条件下反应制得.下列有关说法正确的是( )
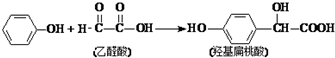
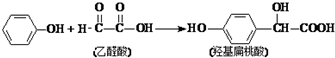
| A. | 该反应是取代反应 | |
| B. | 苯酚和羟基扁桃酸遇上FeCl3溶液都会显色 | |
| C. | 乙醛酸与H2加成的产物能在催化剂作用下形成高分子化合物 | |
| D. | 1mol羟基扁桃酸能与3mol NaOH反应 |
9.下列说法错误的是( )
| A. | 按系统命名法,化合物 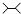 的名称为2,3-二甲基丁烷 的名称为2,3-二甲基丁烷 | |
| B. | 等质量的甲醛、乙酸、葡萄糖完全燃烧耗氧量相等 | |
| C. | 在一定条件下,使煤和氢气作用,可以得到液体燃料 | |
| D. | 聚乙烯(PE)和聚氯乙烯(PVC)的单体都是不饱和烃,均能使溴水褪色 |
16.某溶液中仅含有以下离子中的五种(不考虑水的电离和离子的水解),且各离子的物质的量浓度相等.阳离子:Na+、Mg2+、Fe2+、Al3+、Fe3+;阴离子:OH-、CO32-、Cl-、NO3-、SO42-.下列说法正确的是( )
| A. | 溶液中肯定不存在.的离子是Na+和CO32- | |
| B. | 用氢氧化钠溶液可以确定阳离子的组成 | |
| C. | 溶液中加入稀硫酸,有气体产生 | |
| D. | 溶液中存在的Cl-,可用硝酸酸化的硝酸银溶液检验 |
13.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1.6g甲烷含有的电子数为NA | |
| B. | 1 L0.1 mol/L NaHCO3溶液中含有的HCO3- 数目为0.1 NA | |
| C. | 1 L PH=1的硫酸溶液中含有的H+ 数为0.2 NA | |
| D. | 标准状况下,2.24 LCO和CO2混合气体中含有的氧原子数为0.15NA |
14.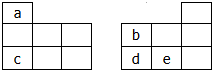 如图均为元素周期表短周期的一部分,其中b的氢化物和它的最高价氧化物对应的水化物能反应生成盐,下列有关a、b、c、d、e五种元素的叙述中,正确的是(0.
如图均为元素周期表短周期的一部分,其中b的氢化物和它的最高价氧化物对应的水化物能反应生成盐,下列有关a、b、c、d、e五种元素的叙述中,正确的是(0.
 如图均为元素周期表短周期的一部分,其中b的氢化物和它的最高价氧化物对应的水化物能反应生成盐,下列有关a、b、c、d、e五种元素的叙述中,正确的是(0.
如图均为元素周期表短周期的一部分,其中b的氢化物和它的最高价氧化物对应的水化物能反应生成盐,下列有关a、b、c、d、e五种元素的叙述中,正确的是(0.| A. | 原子半径:b>c | |
| B. | 由a、b、e三种元素形成的化合物可能是离子化合物 | |
| C. | c与e以原子个数比2:1形成的化合物能促进水的电离 | |
| D. | 氢化物的稳定性:b<d. |