题目内容
14.实验室常用反应NaNO2+NH4Cl=NaCl+N2↑+2H2O制取N2.下列有关说法正确的是( )| A. | NaNO2是氧化剂 | B. | N2的电子式是 | ||
| C. | 生成1 mol N2时转移6 mol 电子 | D. | 氧化剂和还原剂的质量之比是1:1 |
分析 由NaNO2+NH4Cl=NaCl+N2↑+2H2O可知,NaNO2中N元素的化合价由+3价降低为0,NH4Cl中N元素的化合价由-3价升高为0,以此来解答.
解答 解:A.N元素的化合价降低,则NaNO2是氧化剂,故A正确;
B.氮气中存在三键,每个氮原子都满足8电子结构,其电子式为 ,故B错误;
,故B错误;
C.每生成1mol N2时,由化合价的变化可知,转移电子的物质的量为3mol,故C错误;
D.NaNO2中N元素的化合价由+3价降低为0,为氧化剂,NH4Cl中N元素的化合价由-3价升高为0,为还原剂,则氧化剂和还原剂的物质的量之比是1:1,故D错误;
故选A.
点评 本题考查氧化还原反应和电子式,把握氧化还原反应元素的化合价变化为解答的关键,侧重氧化还原反应中基本概念和转移电子的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.下列物质熔化时,不破坏化学键的是( )
| A. | 氧化镁 | B. | 冰 | C. | 金刚石 | D. | 钠 |
5.某种氢氧燃料电池的电解质溶液为硫酸溶液,下列有关该电池的叙述不正确的是( )
| A. | 正极反应式为:O2+2H2O+4e-═4OH- | |
| B. | 工作一段时间后,电解液中硫酸的物质的量不变 | |
| C. | 电解质溶液中H+向正极移动 | |
| D. | 用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.2 mol电子转移 |
2.下列说法正确的是( )
| A. | 淀粉、油脂和蛋白质都是高分子化合物 | |
| B. | 乙酸乙酯和植物油水解均可生成乙醇 | |
| C. | “地沟油”的主要成分是油脂,其类别与煤油不同 | |
| D. | 煤中含有煤焦油及多种化工原料,可通过煤的干馏获得 |
19.关于下列各装置图的叙述中,不正确的是( )
| A. | 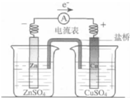 图中总反应为Zn+CuSO4═Cu+ZnSO4 | |
| B. | 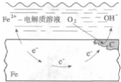 图中正极反应为2H2O+O 2+4e-═4OH- | |
| C. | 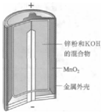 图中负极反应为Zn+2OH--2e-═Zn(OH)2 | |
| D. |  图中向Fe电极区滴入2滴铁氰化钾溶液产生蓝色沉淀 |
6.根据下列实验及现象,能量关系正确的是( )
| 实验及现象 | 能量关系 | |
| A | 将“NO2球”置于热水中,红棕色加深 | N2O4(g)?2NO2(g)△H<0 |
| B | NaOH与HCl溶液混合,溶液温度升高 |  |
| C | 钠投入水中,熔化成小球 |  |
| D | 微热含酚酞的Na2CO3溶液,红色加深 | CO32-(aq)+H2O(l)?HCO3-(aq)+OH-(aq)△H<0 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
3.已知金刚石的燃烧热为395kJ/mol,下表是部分化学键的键能数据.下列选项中正确的是( )
| 化学键 | C-C | O=O | C=O |
| 键能(kJ/mol) | 348 | 498 | x |
| A. | x=794.5 | |
| B. | x=1142.5 | |
| C. | 1mol金刚石的能量一定比1mol CO2能量高 | |
| D. | 金刚石燃烧的热化学方程式为 2C(s)+O2(g)=2CO(g)△H=-790 kJ/mol |
4.下列除杂操作可行的是( )
| A. | 通过浓硫酸除去HCl中的H2O | |
| B. | 通过灼热的镁粉除去N2中的O2 | |
| C. | 制二氧化氮时,用水或NaOH溶液吸收尾气 | |
| D. | 制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体 |
 将0.40mol N2O4气体充入2L固定容积的密闭容器中发生如下反应:N2O4(g)?2NO2(g)△H.在Tl℃和T2℃时,测得NO2的物质的量随时间变化如图所示:
将0.40mol N2O4气体充入2L固定容积的密闭容器中发生如下反应:N2O4(g)?2NO2(g)△H.在Tl℃和T2℃时,测得NO2的物质的量随时间变化如图所示: