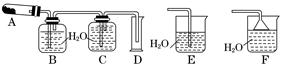题目内容
(1)某兴趣小组在实验室探究工业合成硝酸的化学原理。
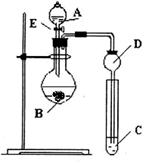
①氨的催化氧化:图a是探究氨的催化氧化的简易装置,实验中观察到锥形瓶中铂丝保持红热,有红棕色气体生成或白烟产生。白烟的成分是 (填化学式)。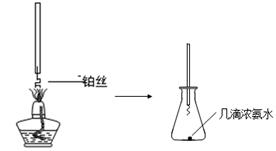
图a 图b
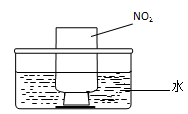
②NO2的吸收:如图b所示,将一瓶NO2倒置于水槽中,在水下移开玻璃片,可观察到的现象是 。
(2)三价铁盐溶液因Fe3+水解而显棕黄色,请以Fe(NO3)3溶液为例,设计实验探究影响盐类水解程度的因素。
①写出Fe(NO3)3水解的离子方程式 。
②参照示例完成下表实验方案的设计。
限选材料:0.05mol?L-1Fe(NO3)3、0.5mol?L-1Fe(NO3)3、1.0mol?L-1HNO3、1.0mol?L-1NaOH、NaHCO3固体、蒸馏水、冰水混合物;pH计及其他常见仪器。
| 可能影响因素 | 实验操作 | 预期现象和结论 |
| 溶液的酸碱性 | 取少量0.5mol?L-1Fe(NO3)3于试管中,加入几滴1mol?L-1HNO3。 | 棕黄色溶液颜色变浅,说明溶液酸性增强能抑制Fe(NO3)3的水解。 |
| 盐的浓度 | | |
| | | |
(1)(共4分)① NH4NO3 (2分)
② 集气瓶中红棕色逐渐消失,集气瓶中的液面逐渐上升 (2分)
(2)(共12分)
① Fe3+ + 3H2O  Fe(OH)3 + 3H+ (2分)
Fe(OH)3 + 3H+ (2分)
②(注:合理的表达或方案也给分,每空2分,共10分)影响条件 实验操作 预期现象和结论 ②盐的浓度 用量筒取10mL Fe(NO3)3于烧杯中,用pH计测出pH值.另取90mL蒸馏水加入烧杯,充分搅拌,再用pH计测出pH值。 前后测得pH值之差小于1。说明加水稀释后平衡右移,生成更多的H+,故增大Fe(NO3)3浓度,抑制Fe(NO3)3水解。 或②盐的浓度 用pH计分别测定0.05mol?L-1Fe(NO3)3和0.5mol?L-1Fe(NO3)3的pH,并比较大小。 二种溶液的pH值之差小于1。说明增大c(Fe(NO3)3),抑制Fe(NO3)3水解。 或②盐的浓度 取少量0.5mol?L-1Fe(NO3)3于试管中加入少量NaHCO3固体。 溶液颜色变深。说明加入少量NaHCO3固体可减少c(H+)促进Fe(NO3)3水解。 或②盐的浓度 取少量0.5mol?L-1Fe(NO3)3于试管中加入几滴1.0mol?L-1NaOH 产生红棕色沉淀,棕黄色溶液变成无色,说明加入NaOH可减少c(H+)能促进Fe(NO3)3水解。 ③升高温度 取少量0.5mol?L-1Fe(NO3)3于试管中,再用酒精灯加热一段时间,观察溶液颜色 加热后溶液颜色变深。说明升高温度促进Fe(NO3)3水解。 或③降低温度 取少量0.5mol?L-1Fe(NO3)3于试管中,再将试管置于放有冰水混合物的烧杯中一段时间,观察溶液颜色 棕黄色溶液颜色变浅。说明降低温度能抑制Fe(NO3)3水解。
解析试题分析:(1)①氨与氧气发生催化氧化,生成NO和水,NO与空气中的氧气反应生成红棕色气体二氧化氮,二氧化氮与水反应又有硝酸生成,硝酸与氨气反应生成白色固体硝酸铵,则白烟的成分是NH4NO3;
②二氧化氮溶于水,生成硝酸和无色气体NO,同时瓶内压强减小,所以看到集气瓶内红棕色气体消失,集气瓶中的液面逐渐上升;
(2)①Fe(NO3)3水解生成氢氧化铁和硝酸,离子方程式为Fe3+ + 3H2O  Fe(OH)3 + 3H+
Fe(OH)3 + 3H+
②影响盐水解程度的因素有浓度、温度。根据铁离子水解的离子方程式判断增大铁离子浓度平衡正向移动,可采用不同浓度的Fe(NO3)3溶液,进行实验,测定溶液的pH,判断水解程度的大小;增大H+ 浓度平衡逆向移动,溶液棕黄色变浅;水解反应可看成是中和反应的逆反应,所以是吸热反应,升高温度平衡,正向移动,溶液棕黄色加深。具体实验如下表:影响条件 实验操作 预期现象和结论 ②盐的浓度 用量筒取10mL Fe(NO3)3于烧杯中,用pH计测出pH值.另取90mL蒸馏水加入烧杯,充分搅拌,再用pH计测出pH值。 前后测得pH值之差小于1。说明加水稀释后平衡右移,生成更多的H+,故增大Fe(NO3)3浓度,抑制Fe(NO3)3水解。 或②盐的浓度 用pH计分别测定0.05mol?L-1Fe(NO3)3和0.5mol?L-1Fe(NO3)3的pH,并比较大小。 二种溶液的pH值之差小于1。说明增大c(Fe(NO3)3),抑制Fe(NO3)3水解。 或②盐的浓度 取少量0.5mol?L-1Fe(NO3)3于试管中加入少量NaHCO3固体。 溶液颜色变深。说明加入少量NaHCO3固体可减少c(H+)促进Fe(NO3)3水解。 或②盐的浓度 取少量0.5mol?L-1Fe(NO3)3于试管中加入几滴1.0mol?L-1NaOH 产生红棕色沉淀,棕黄色溶液变成无色,说明加入NaOH可减少c(H+)能促进Fe(NO3)3水解。 ③升高温度 取少量0.5mol?L-1Fe(NO3)3于试管中,再用酒精灯加热一段时间,观察溶液颜色 加热后溶液颜色变深。说明升高温度促进Fe(NO3)3水解。 或③降低温度 取少量0.5mol?L-1Fe(NO3)3于试管中,再将试管置于放有冰水混合物的烧杯中一段时间,观察溶液颜色 棕黄色溶液颜色变浅。说明降低温度能抑制Fe(NO3)3水解。
考点:考查氨气的催化氧化、二氧化氮的吸收,铁离子的水解及影响水解程度的条件的实验设计

 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是理想,更是一种值得期待的新的生活方式,请运用化学反应原理的相关知识研究碳及其化合物的性质。
(1)近年来,我国储氢纳米碳管研究取得重大进展,用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应化学方程式为:
____C+____K2Cr2O7 + =___CO2↑+ ____K2SO4 + ____Cr2(SO4)3+ ____H2O
请完成并配平上述化学方程式。
其中氧化剂是________________,氧化产物是_________________
(2)甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产。工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
CO(g)+ 2H2(g) CH3OH(g)△H1=-116 kJ·mol-1
CH3OH(g)△H1=-116 kJ·mol-1
①已知: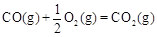 △H2=-283 kJ·mol-1
△H2=-283 kJ·mol-1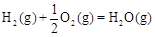 △H3=-242 kJ·mol-1
△H3=-242 kJ·mol-1
则表示1mol气态甲醇完全燃烧生成CO 2和水蒸气时的热化学方程式为 ;
②在容积为1L的恒容容器中,分别研究在230℃、250℃
270℃三种温度下合成甲醇的规律。下图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。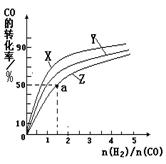
请回答:
ⅰ)在上述三种温度中,曲线Z对应的温度是 。
ⅱ)利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+ 2H2(g) CH3OH(g)的平衡常数K= 。
CH3OH(g)的平衡常数K= 。
③在某温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质的物质的浓度(mol?L-1)变化如下表所示:
| | 0min | 5min | 10min |
| CO | 0.1 | | 0.05 |
| H2 | 0.2 | | 0.2 |
| CH3OH | 0 | 0.04 | 0.05 |
若5min~10min只改变了某一条件,所改变的条件是 ; 且该条件所改变的量是 。
某实验小组同学为了探究铜与浓硫酸的反应,进行了如下实验,实验装置如图所示。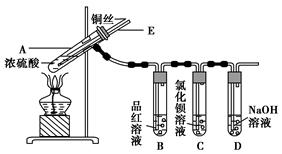
实验步骤:
①先连接如图所示的装置,检查好气密性,再加入试剂;
②加热A试管,待B试管中品红溶液退色后,熄灭酒精灯;
③将Cu丝向上抽动离开液面。
请回答下列问题:
(1)A试管中发生反应的化学方程式为 。
(2)能够证明铜与浓硫酸反应生成气体的实验现象是 。
(3)在盛有BaCl2溶液的C试管中,除了导管口有气泡外,无其他明显现象,若将其中的溶液分成两份,分别滴加下列溶液,将产生沉淀的化学式填入表中对应的位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 | | |
写出其中SO2表现还原性的离子反应方程式: 。
(4)实验完毕后,先熄灭酒精灯,由于导管E的存在,试管B中的液体不会倒吸入试管A中,其原因是 。
(5)实验完毕后,装置中残留的气体有毒,不能打开导管上的胶塞。为了防止该气体排入空气中污染环境,拆除装置前,应当采取的操作是 。
(6)将SO2气体通入含有n mol Na2S的溶液中,充分反应后,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体 mol(不考虑溶解的SO2)。
Na2S2O3·5H2O(俗称海波或大苏打)是照相业常用的一种定影剂。
(一)常用下列途径制备海波:
已知反应:4FeS+7O2  2Fe2O3+4SO2、Na2SO3+S
2Fe2O3+4SO2、Na2SO3+S Na2S2O3
Na2S2O3
(1)计算原料FeS在反应(a)和(b)中的理论分配比:_________。
(2)现有88gFeS,设NaOH溶液吸收SO2的吸收率为96%,问最多制备海波质量为____克(精确到0.1克)
(二)工业上制得的海波晶体中可能含有少量的亚硫酸钠和硫酸钠杂质。为了测定某海波样品的成分,称取三份质量不同的该样品,分别加入相同浓度的硫酸溶液30mL,充分反应后过滤出硫,微热滤液使生成的SO2全部逸出(Na2S2O3+ H2SO4® Na2SO4+ SO2↑+ S↓+ H2O)。测得有关实验数据如下(标准状况):
| | 第一份 | 第二份 | 第三份 |
| 样品的质量/g | 7.54 | 15.08 | 35.00 |
| 二氧化硫的体积/L | 0.672 | 1.344 | 2.688 |
| 硫的质量/g | 0.80 | 1.60 | 3.20 |
(3)计算所用硫酸溶液的物质的量浓度。(写出计算过程)
(4)分析以上实验数据,可判断该样品__________(填字母)
A.不含Na2SO3和Na2SO4 B.不含Na2SO3 含Na2SO4
C.含Na2SO3不含Na2SO4 D.含Na2SO3和Na2SO4
(5)若将30.16g该样品和一定量的上述硫酸溶液混合微热。试讨论:当加入硫酸的体积______(aL)在不同取值范围时,生成SO2体积___________(bL,标态)的值。(可用含a和b的代数式表示)