题目内容
【题目】下列离子方程式书写正确的是
A. 用惰性电极电解MgCl2溶液:2Cl- + 2H2O![]() 2OH-+ H2↑+ Cl2↑
2OH-+ H2↑+ Cl2↑
B. 用银氨溶液检验乙醛中的醛基:CH3CHO+![]() +2OH-
+2OH-![]() CH3COO-+
CH3COO-+![]() +3NH3+2Ag↓+H2O
+3NH3+2Ag↓+H2O
C. 邻羟基苯甲酸中加入足量NaHCO3溶液:

D. 向含NaOH的Cu(OH)2悬浊液中加入乙醛溶液并加热: CH3CHO +2Cu(OH)2+ OH-![]() CH3COO-+ Cu2O↓+3H2O
CH3COO-+ Cu2O↓+3H2O
【答案】BD
【解析】
A. 用惰性电极电解MgCl2溶液的离子反应为2Cl-+Mg2++2H2O![]() Mg(OH)2↓+ H2↑+ Cl2↑,故A错误;
Mg(OH)2↓+ H2↑+ Cl2↑,故A错误;
B. 用银氨溶液检验乙醛中的醛基的离子反应为CH3CHO+2Ag(NH3)![]() +2OH-
+2OH-![]() CH3COO-+NH
CH3COO-+NH![]() +3NH3+2Ag↓+H2O,故B正确;
+3NH3+2Ag↓+H2O,故B正确;
C. 
![]() →H2O+CO2↑ +
→H2O+CO2↑ + 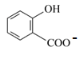 ,故C错误;
,故C错误;
D. 向含NaOH的Cu(OH)2悬浊液中加入乙醛溶液并加热的离子反应为CH3CHO +2Cu(OH)2+OH-![]() CH3COO-+ Cu2O↓+3H2O,故D正确。
CH3COO-+ Cu2O↓+3H2O,故D正确。
故选BD。

【题目】氨是化学实验室及化工生产中的重要物质,应用广泛。N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.2kJ/mol
2NH3(g) ΔH=-92.2kJ/mol
(1)在恒温恒容密闭容器中进行合成氨反应,起始投料时各物质浓度如下表:
N2 | H2 | NH3 | |
投料Ⅰ | 1.0 mol/L | 3.0 mol /L | 0 |
投料Ⅱ | 0.5 mol/L | 1.5 mol/L | 1.0 mol/L |
①按投料Ⅰ进行反应,测得达到化学平衡状态时H2的转化率为40%,则该温度下合成氨反应的平衡常数表达式为_____________。
②按投料Ⅱ进行反应,起始时反应进行的方向为________(填“正向”或“逆向”)。
③若升高温度,则合成氨反应的化学平衡常数________(填“变大”、“变小”或“不变”)。
(2)L(L1、L2)、X可分别代表压强或温度。下图表示L一定时,合成氨反应中H2(g)的平衡转化率随X的变化关系。
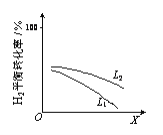
ⅰ X代表的物理量是______。
ⅱ 判断L1、L2的大小关系,并简述理由:______。
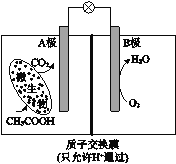
(3)电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如下:
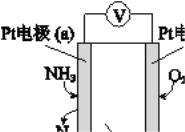
① 电极b上发生的是______反应(填“氧化”或“还原”)
② 写出电极a的电极反应式:_________。