题目内容
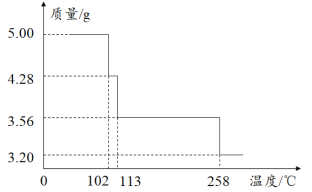
【题目】5.00g CuSO4·5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示:
请回答下列问题:
(1)试确定110℃时固体物质的化学式___________ ;
(2)取200℃所得样品,加热至280℃,该反应的化学方程式为:__________________________________
(3)将280℃所得产物在570℃下灼烧得到的主要产物是1.60g黑色粉末和一种氧化性气体,黑色粉末的化学式为______________ 。
【答案】CuSO4·3H2O CuSO4·H2O ![]() CuSO4 + H2O CuO
CuSO4 + H2O CuO
【解析】
由图分析可知,CuSO45H2O受热到102℃时开始脱水分解,113℃时可得到较稳定的一种中间物,到258℃时才会继续分解;根据相应的化学方程式即可确定此时固体物质的化学式。
(1)设110℃时固体物质的化学式是CuSO4(5-n)H2O;
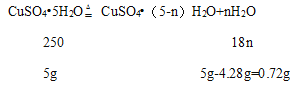
![]() ,解得n=2,
,解得n=2,
110℃时固体物质的化学式是CuSO4·3H2O;
(2)设200℃时固体物质的化学式是CuSO4(5-m)H2O;
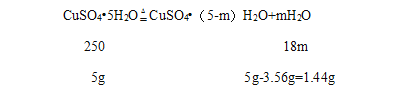
![]() ,解得m=4,
,解得m=4,
200℃时该固体物质的化学式为CuSO4H2O,
设280℃时固体物质的化学式是CuSO4(5-a)H2O;
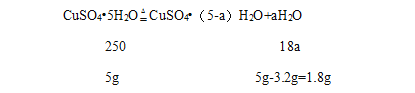
![]() ,解得a=5,
,解得a=5,
280℃时固体物质的化学式是CuSO4;
200℃所得样品,加热至280℃,反应的化学方程式为CuSO4·H2O ![]() CuSO4 + H2O;
CuSO4 + H2O;
(3)CuSO4在570℃下灼烧得到氧化性气体是三氧化硫,根据铜元素守恒,黑色粉末含铜元素![]() ,含有氧元素
,含有氧元素![]() 0.02mol,所以该黑色粉末的化学式是CuO。
0.02mol,所以该黑色粉末的化学式是CuO。

【题目】温度为T℃时,向V L的密闭容器中充入一定量的A和B,发生的反应为A(g)+B(g)![]() C(s)+xD(g) ΔH>0,容器中A、B、D的物质的量浓度随时间的变化如表所示。下列说法不正确的是( )
C(s)+xD(g) ΔH>0,容器中A、B、D的物质的量浓度随时间的变化如表所示。下列说法不正确的是( )
时间 | 0 | 5 min | 10 min | 15 min | 20 min | 25 min | 30 min |
A的物质的量浓度(mol·L-1) | 3.5 | 2.3 | 2.0 | 2.0 | 2.8 | 3.0 | 3.0 |
B的物质的量浓度(mol·L-1) | 2.5 | 1.3 | 1.0 | 1.0 | 1.8 | 2.0 | 2.0 |
D的物质的量浓度(mol·L-1) | 0 | 2.4 | 3.0 | 3.0 | 1.4 | 1.0 | 1.0 |
A.前10 min的平均反应速率v(D)=0.3 mol·L-1·min-1
B.该反应的平衡常数表达式为K=![]()
C.若达到平衡时保持温度不变,压缩容器体积,平衡不移动
D.反应至15 min时,改变的条件可以是降低温度