题目内容
4.下列说法中正确的是( )| A. | 在25℃的纯水中,c(H+)=c(OH-)=10-7 mol/L,呈中性 | |
| B. | 溶液中若c(H+)>10-7 mol/L,则c(H+)>c(OH-),溶液显酸性 | |
| C. | c(H+)越大,则pH值越大,溶液的碱性越强 | |
| D. | pH值为0的溶液中c(H+)=0 mol/L |
分析 A、25℃的纯水中存在离子积常数为10-14,纯水电离出的氢离子和氢氧根离子浓度相同;
B、c(H+)>10-7 mol/L,溶液中氢离子浓度不一定大于氢氧根离子浓度,和溶液温度有关,可能是一定温度下的中性溶液;
C、溶液PH=-lgC(H+),c(H+)越大,则pH值越小;
D、溶液中存在水的电离平衡.
解答 解:A、25℃的纯水中存在离子积常数为10-14,纯水电离出的氢离子和氢氧根离子浓度相同,c(H+)=c(OH-)=10-7 mol/L,呈中性,故A正确;
B、c(H+)>10-7 mol/L,溶液中氢离子浓度不一定大于氢氧根离子浓度,和溶液温度有关,可能是一定温度下的中性溶液;故B错误;
C、(H+)越大,则pH值越小,溶液的酸性越强,故C错误;
D、溶液中存在水的电离平衡,常温下pH值为0的溶液中氢离子浓度为1mol/L,氢氧根离子浓度为10-14,故D错误;
故选A.
点评 本题考查了水的电离平衡应用,溶液酸碱性的判断,主要考查溶液中离子积的计算应用,溶液PH的变化判断,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.对某酸性溶液(可能含有Br-、SO42-、H2SO3、NH4+)分别进行如下实验:
①加热时放出的气体可以使品红溶液褪色 ②加碱调至碱性后,加热时放出的气体可以使湿润的红色
石蕊试纸变蓝 ③加入数滴氯水时,溶液无色,再加入BaCl2溶液时,产生的白色沉淀不溶于稀硝酸.
对于下列物质不能确认其在溶液中是否存在的是( )
①加热时放出的气体可以使品红溶液褪色 ②加碱调至碱性后,加热时放出的气体可以使湿润的红色
石蕊试纸变蓝 ③加入数滴氯水时,溶液无色,再加入BaCl2溶液时,产生的白色沉淀不溶于稀硝酸.
对于下列物质不能确认其在溶液中是否存在的是( )
| A. | Br- | B. | SO42- | C. | H2SO3 | D. | NH4+ |
12.甲烷分子中的4个氢原子全部被苯基取代,可得如图所示的分子,对该分子的描述不正确的是( )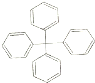

| A. | 分子式为C25H20 | |
| B. | 分子中所有原子有可能处于同一平面 | |
| C. | 该有机物不饱和度为16 | |
| D. | 该物质不属于苯的同系物 |
19.在一定条件下,密闭容器中发生如下反应:2SO2+O2?2SO3,当达到平衡时,通入18O2,再次平衡时,18O存在于( )
| A. | SO2、O2 | B. | SO2、SO3 | C. | SO2、O2、SO3 | D. | O2、SO3 |
9.已知a g气体X2中含有b个X原子,那么c g该气体在273K、1.01×105 Pa条件下的体积是(NA表示阿伏加德罗常数)( )
| A. | $\frac{22.4a•c}{b•{N}_{A}}$L | B. | $\frac{11.2a•b}{c•{N}_{A}}$ L | C. | $\frac{11.2b•c}{a•{N}_{A}}$ L | D. | $\frac{11.2b}{a•c•{N}_{A}}$ L |
16.下列说法不正确的是( )
| A. | 用核磁共振氢谱能区分HCOOCH3和HCOOCH2CH3 | |
| B. | 用红外光谱能区分CH3COOH和CH3COOCH2CH3 | |
| C. | 室温下,在水中的溶解度:苯酚>丙三醇>1-氯丁烷 | |
| D. | 由乙烷和丙烯组成的混合物共1mol,完全燃烧生成3molH2O |
14.下列物质鉴别正确的是( )
| A. | 只要用燃烧的方法就可以鉴别氢气和甲烷 | |
| B. | 闻气味、与金属钠反应、与大理石反应、与新制氢氧化铜反应都可以鉴别酒精和醋酸 | |
| C. | 检验氯乙烷中是否含有氯原子的方法是:氯乙烷与氢氧化钠溶液混合加热片刻后,滴加硝酸银溶液观察是否有白色沉淀 | |
| D. | 检验淀粉水解是否生成葡萄糖的方法是:在水解后的溶液中直接加入新制的氢氧化铜观察是否产生红色沉淀 |