题目内容
14.下列物质鉴别正确的是( )| A. | 只要用燃烧的方法就可以鉴别氢气和甲烷 | |
| B. | 闻气味、与金属钠反应、与大理石反应、与新制氢氧化铜反应都可以鉴别酒精和醋酸 | |
| C. | 检验氯乙烷中是否含有氯原子的方法是:氯乙烷与氢氧化钠溶液混合加热片刻后,滴加硝酸银溶液观察是否有白色沉淀 | |
| D. | 检验淀粉水解是否生成葡萄糖的方法是:在水解后的溶液中直接加入新制的氢氧化铜观察是否产生红色沉淀 |
分析 A.二者燃烧火焰都呈淡蓝色;
B.酒精和醋酸气味不同,乙酸具有酸性,与钠反应时较为剧烈;
C.氯乙烷在氢氧化钠溶液中水解,检验氯离子,应在酸性条件下进行;
D.葡萄糖与氢氧化铜的反应应在碱性条件下进行.
解答 解:A.二者燃烧火焰都呈淡蓝色,不能通过火焰检验,但甲烷燃烧生成二氧化碳,可通入澄清石灰水检验,故A错误;
B.酒精和醋酸气味不同,乙酸具有酸性,可与大理石、氢氧化铜反应,与钠反应时较为剧烈,故B正确;
C.氯乙烷在氢氧化钠溶液中水解,检验氯离子,应在酸性条件下进行,否则生成AgOH而影响实验,故C错误;
D.淀粉在酸性条件下水解生成葡萄糖,但葡萄糖与氢氧化铜的反应应在碱性条件下进行,故D错误.
故选B.
点评 本题考查物质的检验和鉴别,为高频考点,侧重于学生的分析、实验、评价能力的考查,注意把握物质的性质的异同以及实验的严密性、合理性的评价,难度不大.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
4.下列说法中正确的是( )
| A. | 在25℃的纯水中,c(H+)=c(OH-)=10-7 mol/L,呈中性 | |
| B. | 溶液中若c(H+)>10-7 mol/L,则c(H+)>c(OH-),溶液显酸性 | |
| C. | c(H+)越大,则pH值越大,溶液的碱性越强 | |
| D. | pH值为0的溶液中c(H+)=0 mol/L |
5.在强碱性的无色溶液中能大量共存的离子组是( )
| A. | K+、Mg2+、MnO4-、Cl- | B. | Na+、Ba2+、NO3-、Cl- | ||
| C. | Na+、H+、SO42-、Cl- | D. | Ca2+、K+、CO32-、NO3- |
2.下列有关氢氧化铁悬浊液与氢氧化铁胶体的说法正确的是( )
| A. | 都可以发生丁达尔现象 | |
| B. | 分别滴加稀硫酸至过量,现象不同,最终产物相同 | |
| C. | 能透过半透膜 | |
| D. | 分散质颗粒直径都在1~100 nm之间 |
9.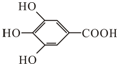 300多年前,著名化学家波义耳发现了铁盐与没食子酸(结构式如图所示)的显色反应,并由此发明了蓝黑墨水,有机物分类中对该物质分类不正确的是( )
300多年前,著名化学家波义耳发现了铁盐与没食子酸(结构式如图所示)的显色反应,并由此发明了蓝黑墨水,有机物分类中对该物质分类不正确的是( )
 300多年前,著名化学家波义耳发现了铁盐与没食子酸(结构式如图所示)的显色反应,并由此发明了蓝黑墨水,有机物分类中对该物质分类不正确的是( )
300多年前,著名化学家波义耳发现了铁盐与没食子酸(结构式如图所示)的显色反应,并由此发明了蓝黑墨水,有机物分类中对该物质分类不正确的是( )| A. | 该物质属于醇 | B. | 该物质属于酚 | ||
| C. | 该物质属于芳香族化合物 | D. | 该物质属于酸 |
19.下列几种物质中不属于天然高分子化合物的是( )
| A. | 聚乙烯 | B. | 淀粉 | C. | 纤维素 | D. | 蛋白质 |
6.在强酸性溶液中能大量共存,且溶液为无色透明的离子组是( )
| A. | Na+、Al3+、SO42-、NO3- | B. | Ba2+、Na+、SO42-、NO3- | ||
| C. | K+、Mg2+、MnO4-、SO42- | D. | K+、Na+、NO3-、HCO3- |
3.下列事实,不能用勒夏特列原理解释的是( )
| A. | 反应CO+NO2?CO2+NO△H<0,升高温度可使平衡向逆反应方向移动 | |
| B. | 合成NH3的反应,为提高NH3的产率,理论上应采取相对较低温度的措施 | |
| C. | 溴水中存在平衡:Br2+H2O?HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅 | |
| D. | 对2HI(g)?H2(g)+I2(g),增大平衡体系的压强(压缩体积)可使体系颜色变深 |