题目内容
7.某铁矿石样品除含SiO2外,主要成分是铁的氧化物.某化学兴趣小组对铁矿石进行探究.(1)探究铁矿石中铁的价态.
①某同学将适量稀硝酸加入少许样品中,加热溶解;取少许溶液,滴加KSCN溶液后出现血红色.由此得出该铁矿石中铁元素价态为+3的结论.你认为此结论不合理(填“合理”或“不合理”),其理由稀硝酸具有强氧化性,能将样品中的+2价的铁元素氧化为+3价.
②请完成下表对铁元素价态的探究实验:
限选试剂:3mol•L-1H2SO4溶液、3% H2O2溶液、6mol•L-1HNO3溶液、0.01mol•L-1KMnO4溶液、稀NaOH溶液、0.1mol•L-1KI溶液、20%KSCN溶液、蒸馏水.
| 实验操作步骤 | 预期现象与结论 |
| 步骤1:用药匙取少许样品于试管中,用滴管滴加适量的3mol•L-1H2SO4溶液,加热,充分反应后得到A溶液 | - |
| 步骤2:取2mLA溶液于试管中,用胶头滴管滴加1~2滴20%KSCN溶液,振荡试管 | 若溶液变红色,样品中含+3价的铁元素 |
| 步骤3:另取2mLA溶液于试管中,用胶头滴管滴加1~2滴0.01mol•L-1KMnO4溶液,振荡试管 | 若溶液的紫红色褪去,样品中含+2价的铁元素 |
将2.25g铁矿石样品经一系列化学处理,制得铁元素全部为Fe2+的待测液250mL,利用反应5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O 对铁矿石中铁元素的含量进行测定.
①取25.00mL待测液进行滴定,平均消耗0.02mol•L-1KMnO4溶液的体积为25.00mL,求铁矿石中铁元素的质量分数(写出计算过程,并保留3位有效数字)
②下列滴定方式中,最合理的是(夹持部分略去)b.

③在滴定过程中,不需要(填“需要”或“不需要”)指示剂来确定滴定终点.
分析 (1)①稀硝酸具有强氧化性,不能利用硝酸溶解;
②检验铁离子用KSCN溶液,若变红色说明含有铁离子;检验亚铁离子,用高锰酸钾溶液,若高锰酸钾褪色,说明含有亚铁离子;
(2)①根据反应5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O,可得出5Fe2+~MnO4-,消耗 MnO4-溶液体积为25.00mL时,求出反应的亚铁离子的物质的量,再求出250mL溶液中亚铁离子的物质的量和质量,再求质量分数;
②酸性溶液或强氧化性溶液应用酸式滴定管盛放;
③KMnO4溶液呈紫色,自身可以作指示剂.
解答 解:(1)①稀硝酸具有强氧化性,不能利用硝酸溶解,稀硝酸能将样品中+2价铁元素氧化为+3价,则不合理,
故答案为:不合理;稀HNO3具有强氧化性,能将样品中+2价铁元素氧化为+3价;
②检验铁离子用KSCN溶液,取2mLA溶液于试管中,用胶头滴管滴加1~2滴20%KSCN溶液,振荡试管,若溶液变红色说明含有铁离子;检验亚铁离子,用高锰酸钾溶液,另取2mLA溶液于试管中,用胶头滴管滴加1~2滴0.01mol•L-1KMnO4溶液,振荡试管,若高锰酸钾褪色,说明含有亚铁离子;
故答案为:
| 实验操作步骤 | 预期现象与结论 |
| 取2mLA溶液于试管中,用胶头滴管滴加1~2滴20%KSCN溶液,振荡试管 | 溶液变红色 |
| 另取2mLA溶液于试管中,用胶头滴管滴加1~2滴0.01mol•L-1KMnO4溶液,振荡试管 | 溶液的紫红色褪去 |
(2)①根据反应5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O,可得出5Fe2+~MnO4-,消耗 MnO4-溶液体积为25.00mL时,则MnO4-物质的量为:0.02mol/L×0.025L=0.0005mol,铁矿石中铁元素的百分含量是:$\frac{0.0005mol×5×56g/mol×\frac{250}{25}}{2.25g}$×100%=62.2%,
答:铁矿石中铁元素的质量分数62.2%;
②酸性溶液或强氧化性溶液应用酸式滴定管,故答案为:b;
③KMnO4溶液呈红色,Fe2+反应完毕,滴入最后一滴KMnO4溶液,紫色不褪去,说明滴定到终点,不需要外加指示剂;
故答案为:不需要.
点评 本题考查了实验设计的基本原理和离子的检验方法、物质含量的测定实验方案设计,题目难度中等,侧重于考查学生的实验探究能力和计算能力,注意把握常见离子的检验方法.

练习册系列答案
相关题目
19.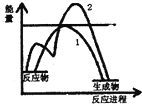 对于CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O反应有关叙述正确的是( )
对于CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O反应有关叙述正确的是( )
 对于CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O反应有关叙述正确的是( )
对于CH3COOH+CH3CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O反应有关叙述正确的是( )| A. | 浓硫酸在该反应中起着降低反应活化能和提高原料转化率作用 | |
| B. | 该反应属于消去反应 | |
| C. | 如图表示放热反应的图象.曲线1表示未加催化剂, 则曲线2表示加了催化剂 | |
| D. | 该反应为放热反应,故升髙温度正反应速度减小,逆反应速度加快 |
2.下列说法正确的是( )
| A. | 胶体区别于其它分散系的本质特征是具有丁达尔现象 | |
| B. | 煤的气化、石油分馏、海水制镁、海带提碘等过程中都包含化学变化 | |
| C. | 棉花和木材的主要成分都是纤维素,蚕丝、羊毛和人造丝的主要成分都是蛋白质 | |
| D. | 甲苯能够被酸性高锰酸钾溶液氧化成苯甲酸,而甲烷不反应,说明苯环能够使甲基变活泼 |
12.电解NO 制备NH4NO3,其工作原理如图所示.下列说法中正确的是( )
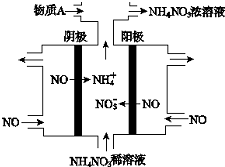

| A. | 阳极上的电极反应为:NO•3e-+4OH-=NO3-+2H2O | |
| B. | 电解生成1 mol NH4NO3 时,转移5NA电子 | |
| C. | 电解质溶液中,NO3-离子向阴极移动 | |
| D. | 为了使电解产物全部转化为NH4NO3,需补充的物质A为稀硝酸 |
19. 实验室常用点滴板来完成部分实验,这样可以节约药品的用量,又便于观察实验现象.图中所示的实验描述的现象正确的是( )
实验室常用点滴板来完成部分实验,这样可以节约药品的用量,又便于观察实验现象.图中所示的实验描述的现象正确的是( )
①装有铜片的孔穴中溶液呈蓝色
②装有胆矾的孔穴中固体的颜色变白
③放有滤纸的孔穴中滤纸变黑
④装有铁片的孔穴中溶液呈浅绿色
⑤装有蛋清溶液的孔穴中呈浅黄色
⑥滴有石蕊溶液的孔穴中溶液变红色.
 实验室常用点滴板来完成部分实验,这样可以节约药品的用量,又便于观察实验现象.图中所示的实验描述的现象正确的是( )
实验室常用点滴板来完成部分实验,这样可以节约药品的用量,又便于观察实验现象.图中所示的实验描述的现象正确的是( )①装有铜片的孔穴中溶液呈蓝色
②装有胆矾的孔穴中固体的颜色变白
③放有滤纸的孔穴中滤纸变黑
④装有铁片的孔穴中溶液呈浅绿色
⑤装有蛋清溶液的孔穴中呈浅黄色
⑥滴有石蕊溶液的孔穴中溶液变红色.
| A. | ①②③⑤ | B. | ①②⑥ | C. | ③⑤⑥ | D. | ②③⑤ |
17.从硫元素的化合价判断,含硫元素的下列物质只作还原剂的是( )
| A. | Na2S | B. | S | C. | S02 | D. | H2SO4 |


 .
. .
.