题目内容
【题目】汽车尾气的主要成分有CO、SO2、NO、NO2等。
(1)利用氨水可以将SO2、NO2吸收,原理如下图所示。
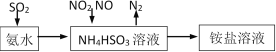
请写出NO2被吸收反应的离子方程式___________________。
(2)科研工作者目前正在尝试以二氧化钛(TiO2)催化分解汽车尾气的研究。
①已知:反应Ⅰ:2NO(g)+O2(g)==2NO2(g) ΔH1 =—113.0 kJ·molˉ1
反应Ⅱ:2SO2(g)+O2(g)==2SO3(1) ΔH2 =—288.4 kJ·molˉ1
反应Ⅲ:3NO2(g)+H2O(g)==2HNO3+NO(g) ΔH3 =—138.0 kJ·molˉ1
则反应NO2(g)+SO2(g)==NO(g)+SO3(1) ΔH4= _______________。
②已知TiO2催化尾气降解原理可表示为:2CO(g)+O2(g) ![]() 2CO2(g) ΔH5; 2H2O(g)+4NO(g)+3O2(g)
2CO2(g) ΔH5; 2H2O(g)+4NO(g)+3O2(g) ![]() 4HNO3(g) ΔH6。
4HNO3(g) ΔH6。
在O2、H2O(g)浓度一定条件下,模拟CO、NO的降解,得到其降解率(即转化率)如图所示。请解释ts后NO降解率下降的可能原因_____________________。
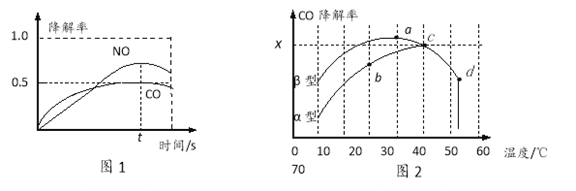
(3)沥青混凝土也可降解CO。如图为在不同颗粒间隙的沥青混凝土(α、β型)在不同温度下,反应相同时间,测得CO降解率变化。结合如图回答下列问题:
①已知在50℃时在α型沥青混凝土容器中,平衡时O2浓度为0.01mol·L—1,求此温度下CO降解反应的平衡常数_______________。
②下列关于如图的叙述正确的是_________________
A.降解率由b点到c点随温度的升高而增大,可知CO降解反应的平衡常数Kb<Kc
B.相同温度下β型沥青混凝土中CO降解速率比α型要大
C.d点降解率出现突变的原因可能是温度升高后催化剂失效
③科研团队以β型沥青混凝土颗粒为载体,将TiO2改为催化效果更好的TiO2纳米管,在10℃~60℃范围内进行实验,请在如图中用线段与“![]() ”阴影描绘出CO降解率随温度变化的曲线可能出现的最大区域范围_____________。
”阴影描绘出CO降解率随温度变化的曲线可能出现的最大区域范围_____________。
(4)TiO2纳米管的制备是在弱酸性水溶液中以金属钛为阳极进行电解,写出阳极的电极反应式 ____________________。
【答案】 2NO2+4HSO3—== N2+4SO42—+4H+ -87.7 kJ·molˉ1 由反应Ⅰ、Ⅲ可知ΔH6=—615.0 kJ·molˉ1,随着反应的进行,反应体系中温度升高,使平衡2H2O+4NO+3O2![]() 4HNO3向逆反应方向移动
4HNO3向逆反应方向移动  B、C 见右图
B、C 见右图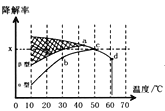 Ti-4e—+2H2O==TiO2+4H+
Ti-4e—+2H2O==TiO2+4H+
【解析】(1)本题考查离子方程式的书写,根据题中所给信息,NO2转化成N2,HSO3-被氧化成SO42-和H+,利用化合价升降法进行配平,即离子方程式为2NO2+4HSO3-= N2+4SO42-+4H+ ;(2)考查热化学方程式的书写,以及影响化学平衡移动的因素,①根据盖斯定律,得到(II-I)/2,△H4=(-288.4+113)/2kJ·mol-1=-87.7kJ·mol-1;②依据I×3+III×2,得出:△H6=(-113×3-138×2)kJ·mol-1=-615kJ·mol-1,CO燃烧是放热反应,随着反应进行温度升高,使2H2O+4NO+3O2 ![]() 4HNO3向逆反应方向进行,因此NO的降解率下降;(3)考查平衡常数的计算、以及影响化学反应速率的因素,①令起始时CO的浓度为1mol·L-1,则达到平衡时c(CO)=(1-x)mol·L-1,c(O2)=0.01mol·L-1,c(CO2)=xmol·L-1,根据平衡常数的定义,K=c2(CO2)/[c2(CO)×c(O2)]=x2/[(1-x)2×0.01]=
4HNO3向逆反应方向进行,因此NO的降解率下降;(3)考查平衡常数的计算、以及影响化学反应速率的因素,①令起始时CO的浓度为1mol·L-1,则达到平衡时c(CO)=(1-x)mol·L-1,c(O2)=0.01mol·L-1,c(CO2)=xmol·L-1,根据平衡常数的定义,K=c2(CO2)/[c2(CO)×c(O2)]=x2/[(1-x)2×0.01]= 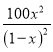 ;②A、化学平衡常数只受温度的影响,CO的燃烧是放热反应,升高温度,平衡向逆反应方向进行,b点温度低于c点温度,因此Kb>Kc,故A错误;B、根据图2,相同温度下β型沥青混凝土中CO降解速率比α型要大,故B正确;C、d点出现突变,CO的降解率降低,可能是温度升高,造成催化剂失效,故C正确;③催化效果好,即加快反应速率,但对化学平衡移动无影响,即图像是
;②A、化学平衡常数只受温度的影响,CO的燃烧是放热反应,升高温度,平衡向逆反应方向进行,b点温度低于c点温度,因此Kb>Kc,故A错误;B、根据图2,相同温度下β型沥青混凝土中CO降解速率比α型要大,故B正确;C、d点出现突变,CO的降解率降低,可能是温度升高,造成催化剂失效,故C正确;③催化效果好,即加快反应速率,但对化学平衡移动无影响,即图像是 ;(4)考查电极反应式的书写,金属钛作阳极,应先失电子,根据电解目的,阳极反应式为Ti-4e-+2H2OTiO2+4H+。
;(4)考查电极反应式的书写,金属钛作阳极,应先失电子,根据电解目的,阳极反应式为Ti-4e-+2H2OTiO2+4H+。

【题目】氯化亚铜常用作有机合成工业中的催化剂,为白色晶体,不溶于乙醇,微溶于水, 易溶于浓盐酸形成络合离子([CuCl2]-)。受潮露置空气中迅速氧化成碱式盐。实验室 用 下列流程制备:
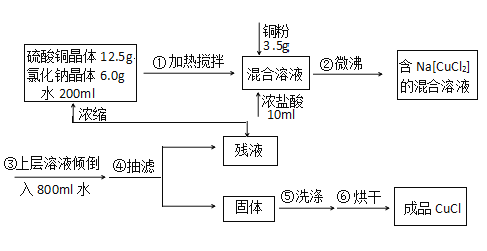
注:Na[CuCl2](易电离,溶液无色)水NaCl+CuCl↓(白色沉淀)。请回答:
(1)写出实验室制取Na[CuCl2]的离子方程式_____________。
(2)判断步骤②反应完全的现象是_______________。
(3)步骤④有关抽滤操作,下列说法正确的是_________。
A. 选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀
B. 在吸滤瓶和抽气泵之间应连接一个安全瓶,吸滤瓶应与安全瓶的长导管相接
C. 抽滤时不宜过滤胶状沉淀,否则易在滤纸上形成一层密实的沉淀
D. 洗涤沉淀时,应关小水龙头,使洗涤剂缓缓通过沉淀物
(4)步骤⑤用乙醇的水溶液洗涤的目的是______________。
(5)步骤⑥烘干须在真空干燥箱中进行,其原因是___________________。
(6)氯化亚铜的定量
①取样品0.25g和10ml过量的FeCl3溶液于250ml锥形瓶中,充分溶解。
②用0.10mol·L-1硫酸锶铈[Ce(SO4)2]标准溶液滴定。
已知:CuCl+FeCl3=CuCl2+FeCl2; Fe2++Ce4+=Fe3++Ce3+
三次平行试验结果如下(平行试验结果相差不能超过1%):
平行试验次数 | 1 | 2 | 3 |
0.25g样品消耗硫酸铈标准溶液的体积(ml) | 24.35 | 24.05 | 23.95 |
则样品中CuCl的纯度为____________。(结果保留三位有效数字)
【题目】Cr、S等元素的化合物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的影响。
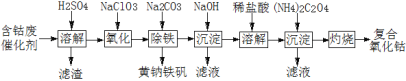
(1)还原沉淀法是处理含铬(Cr2O72和CrO42)工业废水的常用方法,过程如下:
![]()
①已知:常温下,初始浓度为1.0 mol·L1的Na2CrO4溶液中c(Cr2O72)随c(H+)的变化如图所示。则上述流程中CrO42-转化为Cr2O72-的离子方程式为______________________。

②还原过程中氧化剂与还原剂的物质的量之比为__________。
③Cr3+与Al3+的化学性质相似,对CrCl3溶液蒸干并灼烧,最终得到的固体的化学式为____________。
④常温下,Ksp[Cr(OH)3]=1.0×10-32,欲使处理后废水中的c(Cr3+)降至1.0×10-5mol·L1(即沉淀完全),应调节至溶液的pH=_____。
(2)“亚硫酸盐法”吸收烟中的SO2
①将烟气通入1.0mol/L 的Na2SO3溶液,当Na2SO3恰好完全反应时,溶液pH约为3,此时,溶液中各种离子浓度由大到小的顺序为_________(用离子浓度符号和“>”号表示)。
②室温下,将烟道气通入(NH4)2SO3溶液中,测得溶液pH与含硫组分物质的量分数的变化关系如图所示。

已知部分弱电解质的电离常数(25℃)如下:
电解质 | 电离常数 |
H2SO3 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
NH3·H2O | Kb=1.74×10-5 |
(i)(NH4)2SO3溶液呈____(填“酸”、“碱”或“中”)性,其原因是_________________。
(ii)图中b点时溶液pH=7,则n(NH4+):n(HSO3- )=_________。