题目内容
【题目】Cr、S等元素的化合物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的影响。
(1)还原沉淀法是处理含铬(Cr2O72和CrO42)工业废水的常用方法,过程如下:
![]()
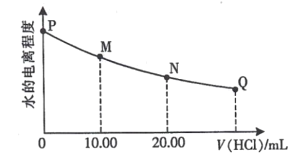
①已知:常温下,初始浓度为1.0 mol·L1的Na2CrO4溶液中c(Cr2O72)随c(H+)的变化如图所示。则上述流程中CrO42-转化为Cr2O72-的离子方程式为______________________。

②还原过程中氧化剂与还原剂的物质的量之比为__________。
③Cr3+与Al3+的化学性质相似,对CrCl3溶液蒸干并灼烧,最终得到的固体的化学式为____________。
④常温下,Ksp[Cr(OH)3]=1.0×10-32,欲使处理后废水中的c(Cr3+)降至1.0×10-5mol·L1(即沉淀完全),应调节至溶液的pH=_____。
(2)“亚硫酸盐法”吸收烟中的SO2
①将烟气通入1.0mol/L 的Na2SO3溶液,当Na2SO3恰好完全反应时,溶液pH约为3,此时,溶液中各种离子浓度由大到小的顺序为_________(用离子浓度符号和“>”号表示)。
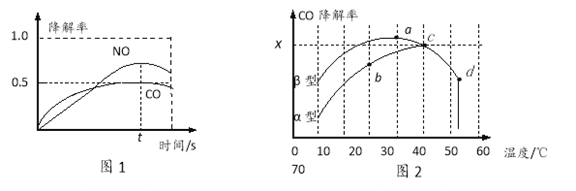
②室温下,将烟道气通入(NH4)2SO3溶液中,测得溶液pH与含硫组分物质的量分数的变化关系如图所示。

已知部分弱电解质的电离常数(25℃)如下:
电解质 | 电离常数 |
H2SO3 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
NH3·H2O | Kb=1.74×10-5 |
(i)(NH4)2SO3溶液呈____(填“酸”、“碱”或“中”)性,其原因是_________________。
(ii)图中b点时溶液pH=7,则n(NH4+):n(HSO3- )=_________。
【答案】CrO42-+2H+![]() Cr2O72-+H2O 1:6 Cr2O3 5 c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-) 碱 H2SO3的第二电离常数Ka2=1.02×10-7小于NH3·H2O的电离常数Kb,故SO32-的水解程度比NH4+的水解程度大,溶液呈碱性 3:1
Cr2O72-+H2O 1:6 Cr2O3 5 c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-) 碱 H2SO3的第二电离常数Ka2=1.02×10-7小于NH3·H2O的电离常数Kb,故SO32-的水解程度比NH4+的水解程度大,溶液呈碱性 3:1
【解析】
(1) ① 从图中可以看出,c(Cr2O72) 随c(H+)的增大而不断增大,当c(H+)=6.0×10-7mol/L时,c(Cr2O72)=0.4mol/L,此时反应达平衡状态,所以此反应为可逆反应。由此可得CrO42-转化为Cr2O72-的离子方程式为CrO42-+2H+![]() Cr2O72-+H2O 答案为CrO42-+2H+
Cr2O72-+H2O 答案为CrO42-+2H+![]() Cr2O72-+H2O
Cr2O72-+H2O
② 依据电子守恒,氧化剂Cr2O72与还原剂Fe2+的关系为:Cr2O72——6Fe2+
从而得出还原过程中氧化剂与还原剂的物质的量之比为1:6。答案为1:6;
③ Cr3+与Al3+的化学性质相似,说明Cr3+在水溶液中易发生水解反应,最终生成Al(OH)3,灼烧时再分解为铬的氧化物。所以对CrCl3溶液蒸干并灼烧,最终得到的固体的化学式为Cr2O3。答案为Cr2O3
④ Ksp[Cr(OH)3]=![]() 1.0×10-32
1.0×10-32
![]() ,pH=5。答案为5;
,pH=5。答案为5;
(2) ① 将烟气通入1.0mol/L 的Na2SO3溶液,当Na2SO3恰好完全反应时,全部生成NaHSO3,此时溶液pH约为3,则表明HSO3-以电离为主。
发生的电离、水解反应方程式为:HSO3-![]() H++SO32-、 HSO3-+H2O
H++SO32-、 HSO3-+H2O![]() H2SO3+OH-、H2O
H2SO3+OH-、H2O![]() H++OH- 且前面反应进行的程度大于后面反应, 从而得出溶液中各种离子浓度由大到小的顺序为c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)。
H++OH- 且前面反应进行的程度大于后面反应, 从而得出溶液中各种离子浓度由大到小的顺序为c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)。
答案为c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)
②(i)在(NH4)2SO3溶液中,NH4+、SO32-都将发生水解,从表中数据Ka2=1.02×10-7、
Kb=1.74×10-5可以看出,HSO3-的电离常数小,SO32-的水解常数大,所以溶液呈碱性。
答案为碱;
溶液呈碱性的原因是:溶液
答案为:H2SO3的第二电离常数Ka2=1.02×10-7小于NH3·H2O的电离常数Kb,故SO32-的水解程度比NH4+的水解程度大,溶液呈碱性。
(ii)图中b点时溶液pH=7,此时c(HSO3-)=c(SO32-),则c(NH4HSO3)=c[(NH4)2SO3],从而得出n(NH4+) :n(HSO3- )= 3:1 答案为3:1。

 同步练习强化拓展系列答案
同步练习强化拓展系列答案