题目内容
【题目】三氯氧磷(POCl3)是一种重要的化工原料,工业上可以直接氧化PCl3制备POCl3,反应原理为:P4(白磷)+6Cl2=4PCl3 2PCl3+O2=2POCl3
PCl3、POCl3的部分性质如下:
熔点/℃ | 沸点/℃ | 其他 | |
PCl3 | -112 | 75.5 | 遇水生成H3PO3和HCl |
POCl3 | 2 | 105.3 | 遇水生成H3PO4和HCl |
某兴趣小组模拟该工艺设计实验装置如下(某些夹持装置、加热装置已略去) :
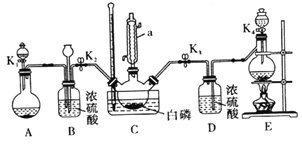
(1)仪器a 的名称为_______________,B装置中长颈漏斗的作用是___________________。
(2)装置E用来制取Cl2,反应的离子方程式为_____________________。
(3)为使实验顺利进行,还需补充的装置为____________________。
(4)反应时,需严格控制三个条件:
①先制取___________,缓慢地通入C 中,直至C 中的白磷消失后,再通入另一种气体。
②C装置用水浴加热控制温度为60 ℃~65℃,除加快反应速率外,另一目的是___________________。
③反应物必须干燥,否则会在C 装置中产生大量的白雾,其主要成分为___________(写化学式)。
(5)反应结束后通过下面步骤测定POCl3产品中Cl 的含量,元素Cl 的质量分数为_______________(写出计算式)。
Ⅰ.取xg产品于锥形瓶中,加入足量NaOH 溶液,POCl3完全反应后加稀硝酸至酸性;
Ⅱ.向锥形瓶中加入0.1000 mol/L 的AgNO3 溶液40.00 mL,使Cl-完全沉淀;
Ⅲ.再向锥形瓶中加入20mL硝基苯,振荡,使沉淀表面被有机物覆盖;
Ⅳ.然后加入指示剂,用c mol/LNH4SCN溶液滴定过量Ag+ 至终点,记下所用体积为VmL。
(己知:AgPO4溶于酸,Ksp(AgCl )=32×10-10,Ksp(AgSCN )=2×10-12)
【答案】 球形冷凝管 平衡气压 4H++2Cl-+MnO2![]() Mn2++Cl2↑+2H2O 在a仪器后连接装有碱石灰的干燥管 Cl2 防止PCl3气化 HCl
Mn2++Cl2↑+2H2O 在a仪器后连接装有碱石灰的干燥管 Cl2 防止PCl3气化 HCl ![]()
【解析】(1) 仪器a的名称是冷凝管(或球形冷凝管),装置A中产生氧气,发生反应的化学方程式为2Na2O2+2H2O==4NaOH+O2↑(或2H2O2![]() 2H2O+O2↑);B装置的作用除观察O2的流速之外,还有平衡气压、干燥O2(或平衡气压和除去水,防止PCl3和POCl3遇水反应引入杂质);正确答案:球形冷凝管; 平衡气压。
2H2O+O2↑);B装置的作用除观察O2的流速之外,还有平衡气压、干燥O2(或平衡气压和除去水,防止PCl3和POCl3遇水反应引入杂质);正确答案:球形冷凝管; 平衡气压。
(2)二氧化锰与浓盐酸加热反应生成氯化锰、氯气和水,反应的离子方程式为:4H++2Cl-+MnO2![]() Mn2++Cl2↑+2H2O;正确答案:4H++2Cl-+MnO2
Mn2++Cl2↑+2H2O;正确答案:4H++2Cl-+MnO2![]() Mn2++Cl2↑+2H2O。
Mn2++Cl2↑+2H2O。
(3)C装置为氯气和磷发生反应的装置,反应结束后会有氯气从冷凝管a中溢出,污染空气,需要吸收处理;同时,POCl3和PCl3遇水会发生反应,为使实验顺利进行,需要在a仪器后连接装有碱石灰的干燥管,防止外界中水蒸气进入C装置内;正确答案:在a仪器后连接装有碱石灰的干燥管。
(4)根据题意可知,要先制备出三氯化磷,然后其被氧化为POCl3,所以先制取氯气,缓慢地通入C中,直至C中的白磷消失后,再通入另一种氧气;正确答案:Cl2。
②由于PCl3的沸点是75.5℃,因此步骤IV控制温度60℃~65℃,其主要目的是加快反应速率,同时防止PCl3气化;正确答案:防止PCl3气化。
③POCl3和PCl3遇水会发生反应,均生成氯化氢,遇到水蒸气产生大量的白雾,所以反应物必须干燥;正确答案:HCl。
(5)根据题意可知,NH4SCN的物质的量为0.001cVmol,则与之反应的银离子的物质的量为0.001cVmol,而总的银离子的物质的量为0.004mol,所以与氯离子反应的银离子的物质的量为0.004mol-0.001cVmol,因此氯离子的物质的量为0.004mol-0.001cVmol,则产品中Cl元素的含量为(0.004-0.001cV)×35.5/x×100%;正确答案:![]() 。
。

【题目】已知A(g)+B(g)C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃ | 700 | 900 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K= , △H0(填“<”“>”“=”);
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003molL﹣1s﹣1 . ,则6s时c(A)= molL﹣1 , C的物质的量为mol;若反应经一段时间后,达到平衡时A的转化率为 , 如果这时向该密闭容器中再充入1mol氩气,平衡时A的转化率为;
(3)判断该反应是否达到平衡的依据为(填正确选项前的字母): a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时问改变 d.单位时间里生成c和D的物质的量相等
(4)1200℃时反应C(g)+D(g)A(g)+B(g)的平衡常数的值为 .