��Ŀ����
����Ŀ����ʽ̼��ͭ������������;�㷺�Ļ���ԭ�ϡ�
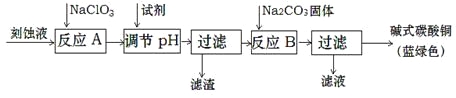
��1����ҵ�Ͽ������Կ�ʴ��Һ����Ҫ�ɷ���Cu2+��Fe2+��Fe3+��H+��Cl���Ʊ���ʽ̼��ͭ�����Ʊ��������£�
��֪��Cu2+��Fe2+��Fe3+���ɳ�����pH���£�
���� | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
��ʼ����pH | 4.2 | 5.8 | 1.2 |
��ȫ����pH | 6.7 | 8.3 | 3.2 |
�������Ƶ������� ��
����ӦA�������Һ��pH��ΧӦΪ ��
����һ�ι��˵õ��IJ�Ʒϴ��ʱ������ж��Ѿ�ϴ���� ��
���������ɫ��Ʒ�л���CuO���ʵ�ԭ���� ��
��2��ijѧϰС����ʵ������������ͼ��ʾװ����ȡ������̽�������ʡ�

��ʵ�����ö������̺�Ũ���������ȡ����������������Ҫ��©���� ��
����C��Ʒ����Һ��ɫ���ܷ�֤��������ˮ��Ӧ�IJ�����Ư���ԣ�˵��ԭ�� ����ʱBװ���з�����Ӧ�����ӷ���ʽ��___________ _____��
��д��A��Һ�о���ǿ���������Ļ�ѧʽ ������A��Һ�м���NaHCO3��ĩ����۲쵽�������� ��
���𰸡���1������Fe2+������Fe3+�����ճ�ȥ����3.2��4.2��
��ȡ���һ��ϴ��Һ��������������ϡ���ᣬ���������������ϴ�Ӹɾ���
����ӦB���¶ȹ��ߡ�
��2������Һ©��
������֤������ΪCl2Ҳ�������ԣ���ʵ����ȷ����Cl2����HClOƯ�ס�
2Fe2����4Br����3Cl2=2Fe3����6Cl����2Br2
�� Cl2HClO ClO-����ɫ�������
��������
���⣨1���û�ѧ�������̵�Ŀ�������Կ�ʴ��Һ����Ҫ�ɷ���Cu2+��Fe2+��Fe3+��H+��Cl���Ʊ���ʽ̼��ͭ�������ȥ��ҺFe2+��Fe3+�����������ݷ��������Ƚ�Fe2+����ΪFe3+������Cu2+���뿪�����������ͼ��������ʴ��Һ���������ƾ���ӦA��Fe2+����ΪFe3+������������֪�����Լ�����pH��3.2��4.2��Fe3+ת��Ϊ�����������������˳�ȥ����Һ�м���̼���ƾ���ӦB���ɼ�ʽ̼��ͭ�����˵ò�Ʒ��������������֪�������Ƶ������ǽ�Fe2+������Fe3+�����ճ�ȥ������ӦA�������Һ��pH��Ŀ���ǽ�������ת��Ϊ����������������ȥ��pH��ΧӦΪ3.2��4.2������һ�ι��˵õ��IJ�ƷΪ�������������溬�������ӵ��������ӡ�ϴ��ʱ���ж��Ѿ�ϴ���ķ�����ȡ���һ��ϴ��Һ��������������ϡ���ᣬ���������������ϴ�Ӹɾ�������ʽ̼��ͭ���ȷֽ���������ͭ���������ɫ��Ʒ�л���CuO���ʵ�ԭ���Ƿ�ӦB���¶ȹ��ߡ���2���� ʵ�����ö������̺�Ũ���������ȡ����Ϊ��Һ�����������װ�ã�����������Ҫ��©���з�Һ©������ ��C��Ʒ����Һ��ɫ������֤��������ˮ��Ӧ�IJ�����Ư���ԣ�ԭ���� ��ΪCl2Ҳ�������ԣ���ʵ����ȷ����Cl2����HClOƯ�ף�C��Ʒ����Һ��ɫ��˵��װ��B�������ѹ�������ʱBװ�����������Ӻ������Ӿ��ѱ�������������Ӧ�����ӷ���ʽ��2Fe2����4Br����3Cl2=2Fe3����6Cl����2Br2 ���� ������ˮ��Ӧ��������ʹ����ᣬ�÷�ӦΪ���淴Ӧ��������Ϊ���ᣬ��A��Һ�о���ǿ���������Ļ�ѧʽCl2 HClO ClO- ������A��Һ�м���NaHCO3��ĩ�������̼�����Ʒ�Ӧ�����Ȼ��ơ�ˮ�Ͷ�����̼����۲쵽������������ɫ���������

 ����ѧУ�ֲ����ܲ�ϵ�д�
����ѧУ�ֲ����ܲ�ϵ�д� �ƸԺ���ȫ�����Ų��Ծ�ϵ�д�
�ƸԺ���ȫ�����Ų��Ծ�ϵ�д�����Ŀ����Ԫ��Ҳ��̼Ԫ��һ������һϵ���⻯��,��NH3��N2H4��N3H5��N4H6�ȡ���ش������й����⣺
��1����������ϵ���⻯���ͨʽΪ____________��
��2����֪��2H2(g)+O2(g)=2H2O(g) ��H=-483.6kJ��mol-1,�����������ϣ���ѧ���������±���
��ѧ�� | H-H | N=N | N-H |
E/kJ��mol-1 | 436 | 946 | 391 |
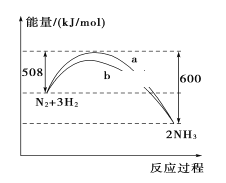
�����ֽⷴӦNH3(g)![]()
![]() N2(g)+
N2(g)+ ![]() H2(g)�Ļ��Ea1=300kJ��mol-1����ϳɰ���Ӧ
H2(g)�Ļ��Ea1=300kJ��mol-1����ϳɰ���Ӧ![]()
![]() N2(g)+
N2(g)+ ![]() H2(g)
H2(g)![]() NH3(g)�Ļ��Ea2=___________��
NH3(g)�Ļ��Ea2=___________��
��������ȫȼ�����ɵ�������̬ˮ���Ȼ�ѧ����ʽΪ__________________________��
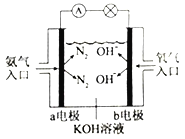
������ͼ�ǰ���ȼ�ϵ��ʾ��ͼ��a�缫�ĵ缫��ӦʽΪ________________��
��3����֪NH3��H2OΪһԪ���N2H4��H2OΪ��Ԫ�����ˮ��Һ�е�һ�����뷽��ʽ��ʾΪ��N2H4��H2O+H2O![]() N2H5��H2O++OH-�����������������(N2H6Cl2)��һ��ˮ������ӷ���ʽΪ__________________;��Һ������Ũ���ɴ�С������˳��Ϊ___________________��
N2H5��H2O++OH-�����������������(N2H6Cl2)��һ��ˮ������ӷ���ʽΪ__________________;��Һ������Ũ���ɴ�С������˳��Ϊ___________________��
��4��ͨ�������ж�(NH4)2SO3��Һ�������(д���������)________________________��(��֪����ˮKb=1.8��10-5;H2SO3 Ka1=1.3��10-2Ka2=6.3��10-8)��
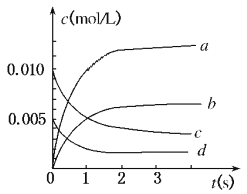
����Ŀ����2 L�ܱ�������,800��ʱ��Ӧ:2NO(g)+O2(g) ![]() 2NO2(g)��ϵ��,n(NO)��ʱ��ı仯���±�:
2NO2(g)��ϵ��,n(NO)��ʱ��ı仯���±�:
ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)д���÷�Ӧ��ƽ�ⳣ������ʽ:K=______________��֪:K300��>K350��,��÷�Ӧ��_______�ȷ�Ӧͼ�б�ʾNO2�仯��������__________������Ӧ�ڵ�5sʱ,NO��ת����Ϊ_________��
(2)��˵���÷�Ӧ�Ѵﵽƽ��״̬����__________
a.v(NO2)=2v(O2)
b.������ѹǿ���ֲ���
c.v��(NO)=2v��(O2)
d.�������ܶȱ��ֲ���
(3)��ʹ�÷�Ӧ�ķ�Ӧ��������,��ƽ��������Ӧ�����ƶ�����__________
a.��ʱ�����NO2����
b.�ʵ������¶�
c.����O2��Ũ��
d.ѡ���Ч����
����Ŀ���±�ΪԪ�����ڱ���һ���֣������Ԫ�آ٣����ڱ��е�λ�ã�����ѧ�����ش��������⣺
�� ���� | IA | 0 | ||||||
1 | �� | ��A | ��A | ��A | ��A | ��A | ��A | |
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | ||||
��1�����ԭ�ӽṹʾ��ͼΪ_________��
��2���ڵ���̬�⻯����ӵĽṹʽΪ_____________��
��3���ڡ��۵���ۺ������������ǿ������˳����________________�����ѧʽ��
��4���ݡ���Ԫ�صĽ�����ǿ������Ϊ___________�������������С�����䡱��
��5���ܡ��ݡ����γɵļ����Ӱ뾶����_______�������������С�����䡱��
��6���١��ܡ���Ԫ�ؿ��γɼȺ����Ӽ��ֺ����ۼ��Ļ����д�����ĵ���ʽ��_______��