题目内容
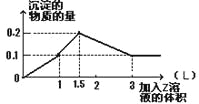
【题目】1 L某混合溶液中,溶质X、Y浓度都为0.1mol·L—1,向混合溶液中滴加0.1 mol·L—1某溶液Z,所得沉淀的物质的量如图所示,则X、Y、Z分别是 ( )
A.偏铝酸钠、氢氧化钡、硫酸
B.氯化铝、氯化镁、氢氧化钠
C.氯化铝、氯化铁、氢氧化钠
D.偏铝酸钠、氯化钡、硫酸
【答案】A
【解析】
A.NaAlO2和Ba(OH)2均为0.1mol,加入等浓度的硫酸,加入的硫酸中的H+和溶液中的OH-生成水,同时SO42-和Ba2+生成BaSO4沉淀,当加入1L硫酸溶液时恰好和Ba(OH)2反应,生成0.1molBaSO4,再加入0.5LH2SO4溶液时,加入的0.1molH+恰好和溶液中的0.1molAlO2-完全反应:H++AlO2-+H2O=Al(OH)3↓,生成0.1molAl(OH)3沉淀。再加入1.5LH2SO4溶液,加入的0.3molH+把生成0.1molAl(OH)3沉淀溶解:Al(OH)3+3H+=Al3++3H2O,和图像相符,故A选;
B.AlCl3和MgCl2均为0.1mol,共需要和0.5mol氢氧化钠反应生成沉淀,即需要5L氢氧化钠溶液才能使沉淀达到最多,和图像不符,故B不选;
C.AlCl3和FeCl3均为0.1mol,共需要0.6molNaOH和它们反应生成沉淀,即需要6LNaOH溶液才能使沉淀达到最多,和图像不符,故C不选;
D.NaAlO2和BaCl2各0.1mol,先加入0.5L硫酸,即0.05mol硫酸,加入的0.1molH+和溶液中的0.1molAlO2-恰好完全反应生成0.1molAl(OH)3沉淀,同时加入的0.05molSO42-和溶液中的Ba2+反应生成BaSO4沉淀。溶液中的Ba2+有0.1mol,加入的SO42-为0.05mol,所以生成0.05molBaSO4沉淀,还剩0.05molBa2+。此时沉淀的物质的量为0.15mol。再加入0.5LH2SO4溶液,加入的0.1molH+恰好把生成的0.1molAl(OH)3沉淀溶解,同时加入的0.05molSO42-恰好和溶液中剩余的0.05molBa2+生成0.05molBaSO4沉淀,此时溶液中的沉淀的物质的量为0.1mol,和图像不符,故D不选。
故选A。

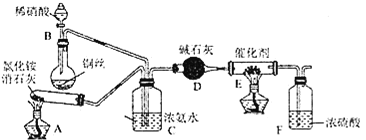
【题目】某学习小组探究稀HNO3、浓HNO3与铜的反应。
装置(尾气处理装置略) | 现象 |
| Ⅰ中开始无明显现象,渐有小气泡生成,越来越剧烈,液面上方出现浅红棕色气体,溶液呈蓝色。 |
Ⅱ中反应剧烈,迅速生成大量红棕色气体,溶液呈绿色。 |
(1)试管Ⅰ中Cu与稀HNO3反应的化学方程式是________。
(2)Ⅱ中反应的速率比Ⅰ中的快,原因是________。
(3)针对Ⅱ中溶液呈绿色的原因,提出假设:
假设1:Cu2+的浓度较大所致;
假设2:溶解了生成的NO2。
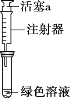
探究如下:取Ⅱ中绿色溶液,分为两等份。
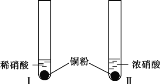
①取一份于如图所示装置中,_______(填“操作”和“现象”),证实Ⅱ中溶解了NO2。
②向另一份溶液加入_____(填化学试剂),溶液变为蓝色。证实假设1不成立,假设2成立。
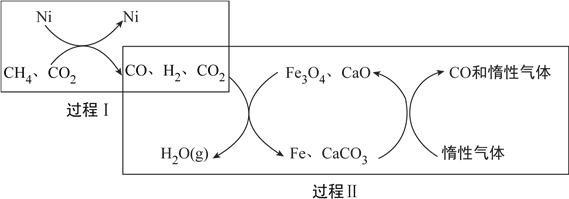
(4)对于稀HNO3与铜生成NO、浓HNO3与铜生成NO2的原因,提出两种解释:
解释1.HNO3浓度越稀,溶液中NO3-的数目越少,被还原时,每个NO3-从还原剂处获得较多电子的机会_____(填“增多”或“减少”),因此被还原为更低价态。
解释2.推测下列平衡导致了产物的不同,并通过如下实验证实了推测的合理性。
3NO2+H2O=2HNO3+NO
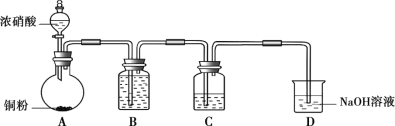
①B中盛放的试剂是________。
②C中盛放Cu(NO3)2和_________。
③该小组证实推测的合理性所依据的实验现象是________。
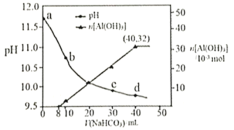
【题目】电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱。25℃时,有关物质的电离平衡常数如下表所示:
化学式 | HF | H2CO3 | HClO |
电离平衡 常数(Ka) | 7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 | 3.0×10-8 |
(1)将浓度为0.1mol·L-1HF溶液加水稀释一倍(假设温度不变),下列各量增大的是___。
A.c(H+) B.c(H+)·c(OH-) C.![]() D.
D.![]()
(2)25℃时,在20mL0.1mol·L-1氢氟酸中加入VmL0.1mol·L-1NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是___。
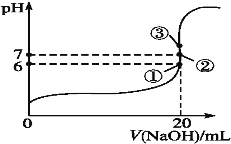
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中c(F-)-c(Na+)=9.9×10-7mol·L-1
C.②点时,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(F-)<c(Na+)=0.1mol·L-1
(3)物质的量浓度均为0.1mol·L-1的下列四种溶液:①Na2CO3溶液;②NaHCO3溶液;③NaF溶液;④NaClO溶液。依据数据判断pH由大到小的是___。
(4)Na2CO3溶液显碱性是因为![]() 水解的缘故,请设计简单的实验事实证之___。
水解的缘故,请设计简单的实验事实证之___。
(5)长期以来,一直认为氟的含氧酸不存在。1971年美国科学家用氟气通过细冰末时获得HFO其结构式为H-O-F。HFO与水反应得到HF和化合物A,每生成1molHF转移___mol电子。