题目内容
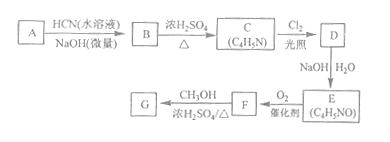
【题目】富马酸(反式丁烯二酸)与Fe2+形成的配合物——富马酸铁又称“富血铁”,可用于治疗缺铁性贫血。以下是合成富马酸铁的一种工艺路线:

回答下列问题:
(1)A的化学名称为_____由A生成B的反应类型为_____。
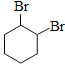
(2)C的结构简式为_____。
(3)富马酸的结构简式为_____。
(4)检验富血铁中是否含有Fe3+的实验操作步骤是_____。
(5)富马酸为二元羧酸,1mol富马酸与足量饱和NaHCO3溶液反应可放出____L CO2(标况);富马酸的同分异构体中,同为二元羧酸的还有____________(写出结构简式)。
【答案】(1)环己烷 取代反应 (每空2分,共4分)
(2)  (2分)
(2分)
(3)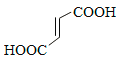 (2分)
(2分)
(4)取少量富血铁,加入稀硫酸溶解,再滴加KSCN溶液,若溶液显血红色,则产品中含有Fe3+;反之,则无。 (2分)
(5)44.8 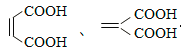 (每空2分,共4分)
(每空2分,共4分)
【解析】
试题分析:18-Ⅱ(1)A的化学名称为环己烷,由环己烷在光照条件下与氯气发生取代反应,生成1—氯环己烷。
(2)环己烯与溴的四氯化碳溶液发生加成反应生成C,C的结构简式为 。
。
(3)丁二烯酸钠酸化得富马酸,其结构简式为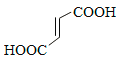 。
。
(4)考查Fe3+的检验。检验富血铁中是否含有Fe3+的实验操作步骤是取少量富血铁,加入稀硫酸溶解,再滴加KSCN溶液,若溶液显血红色,则产品中含有Fe3+;反之,则无。
(5)富马酸为二元羧酸,1mol富马酸与足量饱和NaHCO3溶液反应生成2molCO2,标准状况的体积为44.8L CO2;富马酸的同分异构体中,同为二元羧酸的还有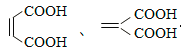 。
。

 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案【题目】下表是元素周期表的一部分, 针对表中的①~⑧种元素,填写下列空白:
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 零 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)上述元素中,化学性质最不活泼的是 (填元素符号)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是 (填元素符号)。
(3)元素②的气态氢化物分子属于 (填电解质或非电解质);元素⑦与④形成化合物的电子式是 。
(4)元素⑤的最高价氧化物与氢氧化钠溶液反应的离子方程式为:
。
(5)元素④的某氧化物可作供氧剂,该氧化物中所含的化学键类型有 ,写出其与二氧化碳反应的化学方程式 。