题目内容
7.下列实验不能达到预期目的是( )| A. | 用饱和食盐水除去Cl2中少量的HCl | |
| B. | 往溴水中通入SO2,可检验SO2的还原性和漂白性 | |
| C. | 往溶液加入盐酸,产生无色无味且能使澄清石灰水浑浊的气体,该气体一定是CO2 | |
| D. | 用硝酸酸化的氯化钡溶液检验某溶液中是否含有SO42- |
分析 A.HCl极易溶于水,饱和氯化钠溶液中含有氯离子,能抑制氯气和水的反应;
B.溴具有强氧化性,能氧化二氧化硫生成硫酸;
C.能使澄清石灰水变浑浊的无色无味气体是二氧化碳;
D.硝酸能将亚硝酸盐氧化生成硫酸根离子.
解答 解:A.HCl极易溶于水,氯气和水反应生成HCl,饱和氯化钠溶液中含有氯离子,所以能抑制氯气和水的反应,则可以用饱和食盐水除去Cl2中少量的HCl,故A不选;
B.溴具有强氧化性,能氧化二氧化硫生成硫酸,所以溴水褪色体现二氧化硫的还原性而不是漂白性,故B选;
C.能使澄清石灰水变浑浊的无色无味气体是二氧化碳,所以往溶液加入盐酸,产生无色无味且能使澄清石灰水浑浊的气体,该气体一定是CO2,故C不选;
D.硝酸能将亚硝酸盐氧化生成硫酸根离子,影响硫酸根离子检验,应该用盐酸酸化的氯化钡溶液检验硫酸根离子,故D选;
故选BD.
点评 本题考查化学实验方案评价,为高频考点,涉及物质性质判断、除杂、离子检验等知识点,明确物质性质是解本题关键,注意:除杂时要除去杂质且不能引进新的杂质,离子检验中要排除其它离子干扰,题目难度不大.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
17. 甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇:
甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇:
CO(g)+2H2(g)?CH3OH (g)
(1)在容积固定为2L的密闭容器内充入1mol CO和2mol H2,加入 催化剂后在250℃开始反应,CO的平衡转化率与温度、压强的关系如图所示.
容器中M、N两点气体的物质的量之比为5:4.
M、N、Q三点的平衡常数KM、KN、KQ的大小关系为KM=KN>KQ.
(2)通过压力计监测上述容器内压强的变化如下:
则从反应开始到20min时,以CO表示的平均反应速率为0.0125mol/(L.min),该温度下平衡常数K=4.
(3)下列描述中能说明上述反应已达平衡状态的是BC.
A.2v(H2)正=v(CH3OH)逆
B.容器内气体的平均摩尔质量保持不变
C.容器中气体的压强保持不变
D.单位时间内生成n mol CO的同时生成2n mol H2
(4)25℃时以甲醇燃料电池(电解质溶液为稀硫酸)为电源电解300mL NaCl溶液,正极反应式为O2+4 H++4 e-=2 H2O.在电解一段时间后,NaCl溶液的pH变为13(假设NaCl溶液的体积不变),则理论上消耗甲醇的物质的量为0.005mol.
 甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇:
甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇:CO(g)+2H2(g)?CH3OH (g)
(1)在容积固定为2L的密闭容器内充入1mol CO和2mol H2,加入 催化剂后在250℃开始反应,CO的平衡转化率与温度、压强的关系如图所示.
容器中M、N两点气体的物质的量之比为5:4.
M、N、Q三点的平衡常数KM、KN、KQ的大小关系为KM=KN>KQ.
(2)通过压力计监测上述容器内压强的变化如下:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/Mpa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
(3)下列描述中能说明上述反应已达平衡状态的是BC.
A.2v(H2)正=v(CH3OH)逆
B.容器内气体的平均摩尔质量保持不变
C.容器中气体的压强保持不变
D.单位时间内生成n mol CO的同时生成2n mol H2
(4)25℃时以甲醇燃料电池(电解质溶液为稀硫酸)为电源电解300mL NaCl溶液,正极反应式为O2+4 H++4 e-=2 H2O.在电解一段时间后,NaCl溶液的pH变为13(假设NaCl溶液的体积不变),则理论上消耗甲醇的物质的量为0.005mol.
18.分子式为C5H10O的有机物,发生银镜反应后,酸化,若不考虑立体异构,其产物的同分异构体既能发生银镜反应,又能与金属钠反应生成氢气有( )
| A. | 12种 | B. | 10种 | C. | 8种 | D. | 14种 |
15.下列试验中,所选装置合理的是( )

| A. | 分离Na2CO3溶液和CH3COOC2H5,选③ | B. | 用CCl4提取碘水中的碘,选② | ||
| C. | 实验室中蒸馏水的制取,选④ | D. | 粗盐提纯,选②和③ |
2.下列现象或事实可用同一化学原理加以说明的是( )
| A. | 氯化铵和碘都可以用加热法进行提纯 | |
| B. | 铜和氯化钠溶液均能导电 | |
| C. | 硫酸亚铁溶液和氢氧化钠溶液在空气中留置均会变质 | |
| D. | 铁片和铝片置于冷的浓硫酸中均无明显现象 |
12.下列有关仪器的使用方法或实验操作不正确的是( )
| A. | 测定溶液pH时,pH试纸先用蒸馏水润湿 | |
| B. | 蒸馏实验中,蒸馏前必须在蒸馏烧瓶中加入碎瓷片 | |
| C. | 用盐酸滴定滴定氨水实验中,用甲基橙作指示剂以减小实验误差 | |
| D. | 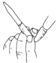 用如图所示的方法排除碱式滴定管胶管中的气泡 用如图所示的方法排除碱式滴定管胶管中的气泡 |
19.岩白菜素具有镇痛、镇静及安定作用等作用,其结构简式如图,下列说法正确的是( )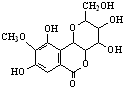

| A. | 能与FeCl3溶液发生显色反应 | |
| B. | 该分子中含有3个手性碳原子 | |
| C. | 该化合物可与Br2发生取代反应 | |
| D. | 1mol该化合物最多可与5molNaOH反应 |
16.下列物质中,既有离子键,又有极性键的是( )
| A. | HCl | B. | KOH | C. | CaCl2 | D. | CH4 |
17.在测定中和热的实验中,下列说法中正确的是( )
| A. | 该实验需要用的主要玻璃仪器有:两个大小相同的烧杯、两只大小相同的量筒、温度计、环形玻璃搅拌棒 | |
| B. | 能用保温杯代替烧杯做有关测定中和热的实验 | |
| C. | 该实验至少需要测定并记录温度的次数是3次 | |
| D. | 若NaOH的物质的量稍大于HCl,会导致所测中和热数值偏高 |