题目内容
16.下列物质中,既有离子键,又有极性键的是( )| A. | HCl | B. | KOH | C. | CaCl2 | D. | CH4 |
分析 活泼金属和活泼非金属元素之间易形成离子键,同种非金属元素之间易形成非极性键,不同非金属元素之间易形成极性键,据此分析解答.
解答 解:A.HCl分子中H-Cl原子之间只存在极性键,故A错误;
B.KOH中钾离子和氢氧根离子之间存在离子键、H-O原子之间存在极性键,故B正确;
C.氯化钙中钙离子和氯离子之间只存在离子键,故C错误;
D.甲烷分子中H-C原子之间只存在极性键,故D错误;
故选B.
点评 本题考查化学键判断,侧重考查基本概念,明确离子键和共价键区别是解本题关键,易错选项是C,注意氯化钙中两个氯离子之间不存在化学键.

练习册系列答案
相关题目
7.下列实验不能达到预期目的是( )
| A. | 用饱和食盐水除去Cl2中少量的HCl | |
| B. | 往溴水中通入SO2,可检验SO2的还原性和漂白性 | |
| C. | 往溶液加入盐酸,产生无色无味且能使澄清石灰水浑浊的气体,该气体一定是CO2 | |
| D. | 用硝酸酸化的氯化钡溶液检验某溶液中是否含有SO42- |
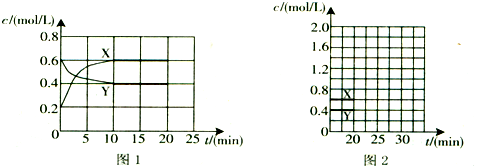
1. 反应2SO2+O2?2SO3经amin后,SO3浓度的变化情况如图所示,在时间0-amin内用O2表示的平均反应速率为0.04mol/(L•min),则a等于( )
反应2SO2+O2?2SO3经amin后,SO3浓度的变化情况如图所示,在时间0-amin内用O2表示的平均反应速率为0.04mol/(L•min),则a等于( )
 反应2SO2+O2?2SO3经amin后,SO3浓度的变化情况如图所示,在时间0-amin内用O2表示的平均反应速率为0.04mol/(L•min),则a等于( )
反应2SO2+O2?2SO3经amin后,SO3浓度的变化情况如图所示,在时间0-amin内用O2表示的平均反应速率为0.04mol/(L•min),则a等于( )| A. | 0.1 | B. | 2.5 | C. | 5 | D. | 10 |
8.加入适量的H2SO4溶液,可使溶液中下列离子的数目显著减少的是( )
| A. | Cl- | B. | Na+ | C. | CO32- | D. | SO42- |
5.X、Y、Z为短周期元素,X原子最外层只有一个电子,Y原子的最外层电子数比内层电子总数少4,Z的最外层电子数是内层电子总数的3倍.下列有关叙述正确的是( )
| A. | Y的价层电子排布式为3s23p5 | |
| B. | 稳定性:Y的氢化物>Z的氢化物 | |
| C. | 第一电离能:Y<Z | |
| D. | X、Y两元素形成的化合物为离子化合物 |
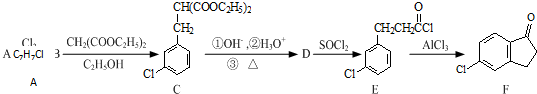
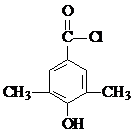 或
或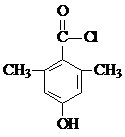 (任写一种).
(任写一种).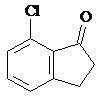 .
.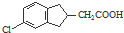 的合成路线流程图(注明反应条件).合成路线流程图示例如下:
的合成路线流程图(注明反应条件).合成路线流程图示例如下:
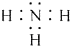 .
.