题目内容
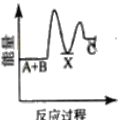
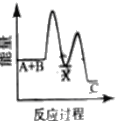
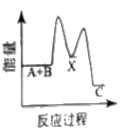
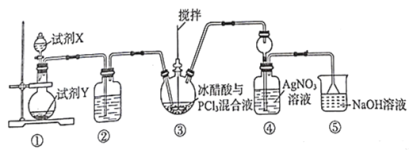
【题目】已知反应![]() 是可逆反应。设计如图装置(
是可逆反应。设计如图装置(![]() 均为石墨电极),分别进行下述操作:
均为石墨电极),分别进行下述操作:
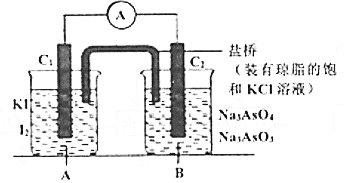
①向B烧杯中逐滴加入浓盐酸。②向B烧杯中逐滴加入![]() 溶液。结果发现电流表指针均发生偏转。
溶液。结果发现电流表指针均发生偏转。
(1)①过程中![]() 棒上发生的反应为_________;
棒上发生的反应为_________;
②过程中![]() 棒上发生的反应为___________。
棒上发生的反应为___________。
(2)操作②过程中,盐桥中的![]() 移向_________烧杯溶液(填“A”或“B”)。
移向_________烧杯溶液(填“A”或“B”)。
资料:![]() 。向
。向![]() 一定浓度的
一定浓度的![]() 溶液中加入
溶液中加入![]() 溶液,达平衡后,相关微粒浓度如下:
溶液,达平衡后,相关微粒浓度如下:
微粒 |
|
|
|
浓度 |
|
| a |
(3)a=________________。该平衡体系中除了含有![]() 和
和![]() 外,判断溶液是否一定还含有其他含碘微粒______________(填“是”或“否”)。
外,判断溶液是否一定还含有其他含碘微粒______________(填“是”或“否”)。
(4)已知:甲醇与水蒸气重整制氢可直接用于燃料电池。
反应:![]()
反应:![]()
则![]() ______________
______________![]()
(5)已知:25℃时,![]() 。医学上进行消化系统的X射线透视时,常使用
。医学上进行消化系统的X射线透视时,常使用![]() 作内服造影剂。胃酸酸性很强(pH约为1),但服用大量
作内服造影剂。胃酸酸性很强(pH约为1),但服用大量![]() 仍然是安全的,
仍然是安全的,![]() 不溶于酸的原因是(用溶解平衡原理解释):_________。误服少量
不溶于酸的原因是(用溶解平衡原理解释):_________。误服少量![]() ,应尽快用大量的一定浓度的
,应尽快用大量的一定浓度的![]() 溶液给患者洗胃,忽略洗胃过程中
溶液给患者洗胃,忽略洗胃过程中![]() 溶液浓度的变化,要使残留在胃液中的
溶液浓度的变化,要使残留在胃液中的![]() 浓度为
浓度为![]() ,应服用的
,应服用的![]() 溶液的最低浓度为_______
溶液的最低浓度为_______![]() 。
。
【答案】![]()
![]() A
A ![]() 是
是 ![]()
![]() 不能减少
不能减少![]() 或
或![]() 的浓度,平衡不能向溶解的方向移动
的浓度,平衡不能向溶解的方向移动 ![]()
【解析】
根据加入溶液酸碱性的不同判断反应进行的方向;根据化学平衡常数计算反应反应中某一物质的浓度,根据元素的守恒定律判断溶液中是否存在其他微粒;根据盖斯定律计算化学反应热;根据化学平衡移动原理分析平衡是否发生移动。
(1)过程①向烧杯B中加入浓盐酸,反应正向进行,C1棒上溶液中的碘离子失电子生成I2,电极方程式为2I--2e-= I2,C2棒上溶液中的![]() 得电子生成
得电子生成![]() ,电极方程式为
,电极方程式为![]() +2e-+2H+=
+2e-+2H+=![]() +H2O;过程②向烧杯B中加入NaOH溶液,反应逆向进行,其总反应相应变为
+H2O;过程②向烧杯B中加入NaOH溶液,反应逆向进行,其总反应相应变为![]() + I2+2OH-=
+ I2+2OH-=![]() + H2O+2I-,C1棒上溶液中I2得电子生成I-,电极方程式为I2+2e-=2I-,C2棒上溶液中
+ H2O+2I-,C1棒上溶液中I2得电子生成I-,电极方程式为I2+2e-=2I-,C2棒上溶液中![]() 失电子生成
失电子生成![]() ,电极方程式为
,电极方程式为![]() -2e-+2OH-=
-2e-+2OH-=![]() + H2O;
+ H2O;
(2)过程②A烧杯中生成大量I-,导致盐桥中K+向A烧杯移动;
(3)根据反应可写出反应的化学平衡常数表达式K=![]() =640,将碘离子和碘单质的浓度带入,解得c(
=640,将碘离子和碘单质的浓度带入,解得c(![]() )=4×10-3mol/L;对于方程式I-+I2=
)=4×10-3mol/L;对于方程式I-+I2=![]() ,根据平衡时三种物质的平衡浓度可以计算这个反应中I的总物质的量浓度为1.95×10-2mol/L,物质的量为1.95×10-2×30×10-3=5.85×10-4mol,而反应前碘化钾溶液中碘离子的物质的量为0.1×10×10-3=10-3mol,二者存在差值,说明溶液中还含有其他含碘微粒;
,根据平衡时三种物质的平衡浓度可以计算这个反应中I的总物质的量浓度为1.95×10-2mol/L,物质的量为1.95×10-2×30×10-3=5.85×10-4mol,而反应前碘化钾溶液中碘离子的物质的量为0.1×10×10-3=10-3mol,二者存在差值,说明溶液中还含有其他含碘微粒;
(4)根据盖斯定律,将第一个热化学方程式与第二个热化学方程式相加即得到第三个方程式的反应热,第三个热化学方程式的反应热H3=H1+H2=+90.64 kJ/mol+41.20 kJ/mol=+131.84 kJ/mol;
(5)人胃液的主要成分为HCl,服用BaSO4后不会对人体造成伤害,原因是H+不能减少钡离子或硫酸根的浓度,硫酸钡的沉淀溶解平衡不会发生移动;洗胃过程中要使残留在胃中的Ba2+浓度小于2×10-10mol/L,根据BaSO4的溶度积常数可以计算硫酸根浓度c(![]() )=
)=![]() =
=![]() =0.5mol/L,故应服用硫酸钠溶液的最低浓度为0.5mol/L。
=0.5mol/L,故应服用硫酸钠溶液的最低浓度为0.5mol/L。

【题目】氮化硼![]() 广泛应用于制造合金、耐高温材料和半导体。科研小组以富硼废料(主要成分为
广泛应用于制造合金、耐高温材料和半导体。科研小组以富硼废料(主要成分为![]() 和
和![]() ,还含有少量
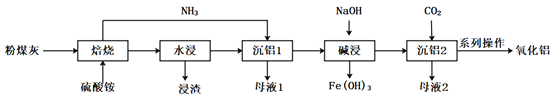
,还含有少量![]() 等)为原料,制备氮化硼的一种工艺流程如下:
等)为原料,制备氮化硼的一种工艺流程如下:
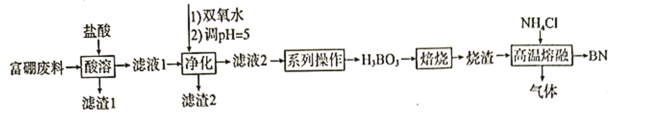
已知:硼酸溶于水和乙醇,在水中的溶解度如下
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度( | 2.77 | 4.78 | 8.90 | 14.89 | 23.54 | 39.60 |
回答下列问题:
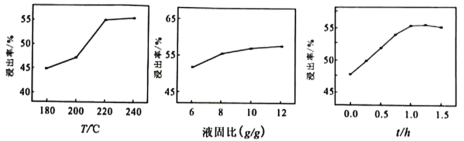
(1)“酸溶”时需控制适当温度,温度不能过高的原因为____________________________;除控制适当温度外,可加快“酸溶”速率的措施还有__________________(答出一点即可)。
(2)“净化”时第一步反应的化学方程式为__________________;第二步调![]() 的目的为_______________;滤液2中
的目的为_______________;滤液2中![]() _______________(已知
_______________(已知![]() )
)
(3)“系列操作”中,洗涤结晶出来的硼酸的操作为__________________________。
(4)“高温熔融”过程中生成的气体为两种氢化物,则主要反应的化学方程式为__________________________;生成的气体用水吸收后可返回__________________________工序循环利用。
【题目】下列实验中,现象及结论都正确,且二者之间有因果的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 将少量Na2SO3样品溶于水,滴加足量盐酸酸化的Ba(NO3)2溶液 | 有白色沉淀产生 | Na2SO3已变质 |
B | 将AlCl3溶液加热蒸干 | 得到白色固体 | 成分为纯净的AlCl3 |
C | 蘸有浓氨水的玻璃棒靠近X | 有白烟产生 | X一定是浓盐酸 |
D | 常温下,向等体积、等浓度的NaHCO3和CH3COONa溶液中分别滴加2滴酚酞 | 两份溶液均变红,NaHCO3溶液红色更深 | 常温下的水解平衡常数: |
A.AB.BC.CD.D