题目内容
11.短周期元素W、X、Y和Z的原子序数依次增大.元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍.下列说法错误的是( )| A. | 元素X与氢形成的原子比为1:1的化合物有很多种 | |
| B. | 元素W、X的氯化物中,各原子均满足8电子的稳定结构 | |
| C. | 元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 | |
| D. | 元素Z可与元素X形成共价化合物XZ2 |
分析 因X原子的最外层电子数是内层电子数的2倍,是C元素,Y是地壳中含量最丰富的金属元素,为Al元素.Z原子的最外层电子数是其电子层数的2倍,是短周期元素,且W、X、Y和Z的原子序数依次增大,Z为S元素,W是制备一种高效电池的重要材料,是Li元素,据此分析.
解答 解:因X原子的最外层电子数是内层电子数的2倍,是C元素,Y是地壳中含量最丰富的金属元素,为Al元素.Z原子的最外层电子数是其电子层数的2倍,是短周期元素,且W、X、Y和Z的原子序数依次增大,Z为S元素,W是制备一种高效电池的重要材料,是Li元素;
A、元素X与氢形成的化合物有C2H2、C6H6等,故A正确;
B、W、X的氯化物分别为LiCl和CCl4,则Li+的最外层只有两个电子,不满足8电子的稳定结构,故B错误;
C、元素Y为铝,铝与氢氧化钠溶液或盐酸反应均有氢气生成,故C正确;
D、硫和碳可形成共价化合物CS2,故D正确;
故选B.
点评 本题考查元素的推断和元素的性质,充分利用原子结构的知识是解题的关键,注意把握常见元素及其化合物的性质,题目难度不大.

练习册系列答案
相关题目
1.下列有关溶液的叙述正确的是( )
| A. | 惰性电极电解氯化钾溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| B. | 能溶解Fe(OH)3的溶液中含有:HCO3-、Na+、Mg2+、Cl- | |
| C. | 中性溶液中可能大量存在Fe3+、K+、Cl-、SO42- | |
| D. | 石灰乳与Na2CO3溶液混合:Ca2++CO32-=CaCO3↓ |
2.化学式为C3H7FO的物质,含有羟基的同分异构体数目为(不考虑空间异构)( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
19.有一种基于乙醇酸性燃料电池原理设计的酒精检测仪,其原理是通过将乙醇氧化为乙酸来测定血液中乙醇的含量.下列有关说法正确的是( )
| A. | 电池工作时消耗5.6LO2,转移电子为1mol | |
| B. | 检测时,电解质溶液中的H+向负极移动 | |
| C. | 正极上发生的反应为:O2+4e-+2H2O=4OH- | |
| D. | 负极上发生的反应为:CH3CH2OH-4e-+H2O=CH3COOH+4H+ |
16.用下列实验装置进行相应的实验,不能达到实验目的是( )
| A | B | C | D | |
| 装置 | 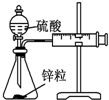 | 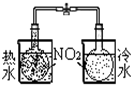 | 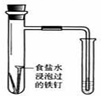 | 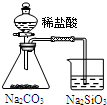 |
| 实验 | 结合秒表定量比较锌与不同浓度的稀硫酸反应的快慢 | 证明温度对化学平衡的影响 | 验证铁钉发生吸氧腐蚀 | 可证明非金属性Cl>C>Si |
| A. | A | B. | B | C. | C | D. | D |
3.下列有关图示分析正确的是( )
| A. |  如图所示,集气瓶内充满Cl2和CH4的混合气体或NO2和O2的混合气体,置于光亮处,将滴管内的水挤入集气瓶后,烧杯中的水会进入集气瓶,并可能充满集气瓶 | |
| B. | 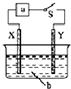 如图所示,X为铁棒,Y为铜棒,a为直流电源,当S闭合后,当b为NaOH溶液,X极附近产生白色沉淀时,电子从X极流入a | |
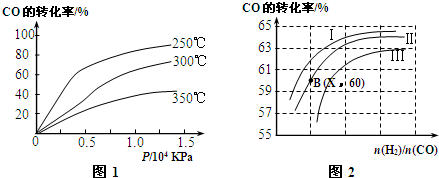
| C. | 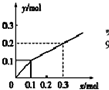 Pt为电极,电解含0.10 mol M+和0.1 mol N3+(M+、N3+均为金属阳离子)的溶液,阴极析出金属单质或气体的总物质的量(y)与导线中通过电子的物质的量(x)的关系如图,离子氧化能力M+>N3+>H+ | |
| D. | 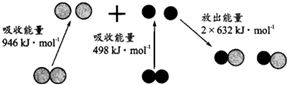 如图为N2(g)和O2(g)生成NO(g)过程中的能量变化,则N≡N的键能为946kJ/mol,热化学方程式为:N2(g)+O2(g)═2NO(g)△H=-180 kJ/mol |
20.我省近年来以铁矿石为原料的产业发展迅猛,下列有关说法正确的是( )
| A. | 以焦炭和铁矿石为原料炼铁的原理是用焦炭直接还原化合态的铁 | |
| B. | 据报道,庐江磁性材料产生“磁”力无穷,磁性氧化铁的化学式是Fe2O3 | |
| C. | 为证明某铁矿石中存在铁离子,可将铁矿石溶于硝酸后,再加KSCN溶液 | |
| D. | 利用铁矿石制得的能除去污水中的,可知相同条件下,Ksp(FeS)>Ksp(HgS) |