题目内容
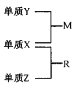
【题目】短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5。X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和;Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X和Z可以形成XZ3的化合物。请回答:
(1)Y元素的名称是____________。
(2)XZ3化合物的电子式是______________ 分子的立体构型_______________
(3)分别写出X、Y的最高价含氧酸的分子式_____________、______________。
【答案】碳 ![]() 三角锥形 HNO3 H2CO3
三角锥形 HNO3 H2CO3
【解析】
Y元素原子的最外电子层上的电子数是它的电子层数的2倍,Y为碳元素;短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5,X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和,X和Z可以形成XZ3的化合物,则X为N元素,Z为H元素;结合相关化学用语作答。
Y元素原子的最外电子层上的电子数是它的电子层数的2倍,Y为碳元素;短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5,X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和,X和Z可以形成XZ3的化合物,则X为N元素,Z为H元素;
(1)Y元素的名称是碳;答案是:碳;
(2) XZ3的化学式为NH3,氨气是共价化合物,其电子式为![]() ;NH3分子中N上的孤电子对数为
;NH3分子中N上的孤电子对数为![]() ×(5-3×1)=1,σ键电子对数为3,价层电子对数为4,VSEPR模型为四面体型,NH3分子构型为三角锥形;
×(5-3×1)=1,σ键电子对数为3,价层电子对数为4,VSEPR模型为四面体型,NH3分子构型为三角锥形;
答案是:![]() ;三角锥形;
;三角锥形;
(3)氮元素的最高价为+5价,碳元素的最高价为+4价,则氮元素和碳元素的最高价含氧酸的分子式为: HNO3、H2CO3;
答案是:HNO3、H2CO3。

 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案