题目内容
7.下列事实能用勒夏特列原理解释的是( )| A. | 实验室采用排饱和食盐水的方法收集Cl2 | |
| B. | 500℃左右的温度比室温更有利于合成氨反应 | |
| C. | H2、I2、HI平衡混合气体加压后颜色加深 | |
| D. | SO2氧化为SO3,往往需要使用催化剂 |
分析 平衡移动原理是如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动,平衡移动原理适用的对象应存在可逆过程,如与可逆过程无关,则不能用平衡移动原理解释,平衡移动原理对所有的动态平衡都适用.
解答 解:A.氯气能够溶于水,存在Cl2+H2O?HClO+H++Cl-,食盐水中含有大量氯离子,促使平衡逆向移动,降低氯气在食盐水中的溶解度,可以用勒夏特列原理解释,故A选;
B.合成氨的正反应是放热反应,升高温度平衡逆向移动,但500℃左右的温度比室温更有利于合成氨反应,不能用平衡移动原理解释,故B不选;
C.该反应前后气体物质的量之和不变,所以压强不影响平衡移动,不能用平衡移动原理解释,故C不选;
D.催化剂只影响反应速率不影响平衡移动,所以不能用平衡移动原理解释,故D不选;
故选A.
点评 本题考查化学平衡移动原理,为高频考点,明确平衡移动原理内涵及适用范围是解本题关键,注意催化剂不影响平衡移动,易错选项是D.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
18.我国科学家研发成功了甲烷和二氧化碳的共转化技术,利用分子筛催化剂高效制得乙酸.下列有关说法正确的是( )
| A. | 所有反应物和产物中都既含极性键又含非极性键 | |
| B. | 消耗22.4L CO2可制得乙酸60g | |
| C. | 该反应不是氧化还原反应 | |
| D. | 该反应过程符合“绿色化学”原理,原子利用率达100% |
15.下列热化学方程式表述正确的是(△H的绝对值均正确)( )
| A. | NaOH(aq)+HNO3(aq)═NaNO3(aq)+H2O(l)△H=+57.3kJ/mol(中和热) | |
| B. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1367.0kJ/mol(燃烧热) | |
| C. | S(s)+O2(g)═SO2(g)△H=-269.8kJ/mol(反应热) | |
| D. | 2NO2═O2+2NO△H=+116.2kJ/mol(反应热) |
2.下列有关叙述正确的是( )
| A. | 在中和滴定实验中,滴定管用蒸馏水洗涤后,再用标准液润洗,再加进标准液 | |
| B. | 若用50mL 0.55mo1•L-1的氢氧化钠溶液,分别与50mL 0.50mo1•L-1的盐酸和 50mL0.50mo1•L-1的硫酸充分反应,两反应测定的中和热不相等 | |
| C. | 如图装置所示,可准确测定中和热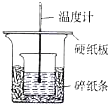 | |
| D. | 进行中和滴定操作时,左手震荡锥形瓶,右手转动活塞控制液滴流速,眼睛要始终注视滴定管内溶液液面的变化 |
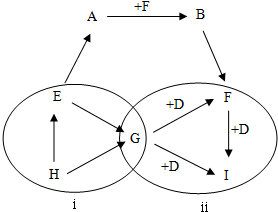
12.A、B、C、D四种物质均为下列离子组成的可溶性化合物,组成这四种物质的离子(离子不能重复组合)有:
分别取四种物质进行实验,实验结果如下
①B溶液分别与C、D混合,均有白色沉淀生成;
②将A溶液逐滴滴入C溶液中,有沉淀生成,继续滴加A溶液时,沉淀减少直至完全消失;
③A与D两种固体混合加热有气体生成,该气体能使湿润的红色石蕊试液变蓝;
④用石墨电极电解B溶液,在阳极上产生一种有刺激性气味的气体.
(1)A所含的阴离子的电子式是 ,B所含的阳离子是Ba2+.
,B所含的阳离子是Ba2+.
(2)C的化学式是Al2(SO4)3,D的化学式是(NH4)2CO3.
(3)写出②中沉淀溶解的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
| 阳离子 | Na+、Al3+、Ba2+、NH4+ |
| 阴离子 | Cl-、OH-、CO32-、SO42- |
①B溶液分别与C、D混合,均有白色沉淀生成;
②将A溶液逐滴滴入C溶液中,有沉淀生成,继续滴加A溶液时,沉淀减少直至完全消失;
③A与D两种固体混合加热有气体生成,该气体能使湿润的红色石蕊试液变蓝;
④用石墨电极电解B溶液,在阳极上产生一种有刺激性气味的气体.
(1)A所含的阴离子的电子式是
 ,B所含的阳离子是Ba2+.
,B所含的阳离子是Ba2+.(2)C的化学式是Al2(SO4)3,D的化学式是(NH4)2CO3.
(3)写出②中沉淀溶解的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
20.高铁酸盐(K2FeO4)在能源、环保等方面有着广泛的用途.湿法、干法制备高铁酸盐的原理如下表所示.
(1)写出干法制备K2FeO4 的化学方程式为,Fe2O3+3KNO3+4KOH$\frac{\underline{\;\;△\;\;}}{\;}$2K2FeO4+3KNO2+2H2O,该反应中氧化剂与还原剂的物质的量之比为3:1.
(2)高铁酸钾在水中既能消毒杀菌,又能净水,是一种理想的水处理剂.它能消毒杀菌是因为高铁酸钾有强氧化性,它能净水的原因是高铁酸钾与水反应生成的Fe(OH)3胶体有吸附性.
(3)在实验室配置Fe(NO3)3溶液时,若用蒸馏水直接配置,所得溶液往往较混浊,其原因是(用离子方程式表示)Fe3++3H2O?Fe(OH)3+3H+,因此,正确的配置操作是在溶液中加入少量的(填试剂名称)硝酸,其目的是抑制铁离子的水解.
(4)Fe2O3是一种红棕色的氧化物,写出它和盐酸反应的离子方程式Fe2O3+6H+=3H2O+2Fe3+.
(5)检验Fe3+ 的方法很多,写出其中的一种检验方法取少量溶液于试管中,加入少量KSCN溶液,如果变成血红色溶液,则含有Fe3+.
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
(2)高铁酸钾在水中既能消毒杀菌,又能净水,是一种理想的水处理剂.它能消毒杀菌是因为高铁酸钾有强氧化性,它能净水的原因是高铁酸钾与水反应生成的Fe(OH)3胶体有吸附性.
(3)在实验室配置Fe(NO3)3溶液时,若用蒸馏水直接配置,所得溶液往往较混浊,其原因是(用离子方程式表示)Fe3++3H2O?Fe(OH)3+3H+,因此,正确的配置操作是在溶液中加入少量的(填试剂名称)硝酸,其目的是抑制铁离子的水解.
(4)Fe2O3是一种红棕色的氧化物,写出它和盐酸反应的离子方程式Fe2O3+6H+=3H2O+2Fe3+.
(5)检验Fe3+ 的方法很多,写出其中的一种检验方法取少量溶液于试管中,加入少量KSCN溶液,如果变成血红色溶液,则含有Fe3+.