题目内容
2.2-甲基-1,3-丁二烯和足量的溴发生加成反应,其加成产物有(不考虑立体异构)( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
分析 2-甲基-1,3-丁二烯结构简式为CH2=C(CH3)CH=CH2,与足量溴发生加成反应,可能是1,2-加成、可能是3,4-加成,也可能是1,4-加成,也可能是1、2、3、4-加成,据此分析解答.
解答 解:2-甲基-1,3-丁二烯结构简式为CH2=C(CH3)CH=CH2,与足量溴发生加成反应,可能是1,2-加成、可能是3,4-加成,也可能是1,4-加成,也可能是1、2、3、4-加成,所以其加成产物有4种,故选D.
点评 本题考查有机物结构和性质,为高频考点,明确二烯烃发生加成特点是解本题关键,注意不能漏掉加成情况,为易错题.

练习册系列答案
相关题目
17.下列有关说法正确的是( )
| A. | SiO2既可与NaOH溶液反应也可与HF溶液反应,所以SiO2属于两性氧化物 | |
| B. | SO2溶于水后,其水溶液可以导电,所以SO2属于电解质 | |
| C. | 当光束照射云、烟、雾时,均可看到明显的光路,是因为三者都属于胶体 | |
| D. | 14CO2和12CO2具有相同的元素组成,所以14CO2、12CO2属于同素异形体 |
14.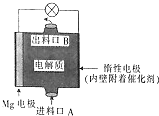 镁燃料电池是一种环境友好型的高性能电源,如图是Mg-NaClO燃料电池的示意图,电池总反应为Mg+ClO-+H2O═Cl-+Mg(OH)2↓,下列判断不正确的是( )
镁燃料电池是一种环境友好型的高性能电源,如图是Mg-NaClO燃料电池的示意图,电池总反应为Mg+ClO-+H2O═Cl-+Mg(OH)2↓,下列判断不正确的是( )
 镁燃料电池是一种环境友好型的高性能电源,如图是Mg-NaClO燃料电池的示意图,电池总反应为Mg+ClO-+H2O═Cl-+Mg(OH)2↓,下列判断不正确的是( )
镁燃料电池是一种环境友好型的高性能电源,如图是Mg-NaClO燃料电池的示意图,电池总反应为Mg+ClO-+H2O═Cl-+Mg(OH)2↓,下列判断不正确的是( )| A. | 惰性电极是该电池的正极 | |
| B. | 电解质中的多数ClO-向电池的负极移动 | |
| C. | 电池中发生的还原反应是Mg2++ClO-+H2O+2e-═Cl-+Mg(OH)2↓ | |
| D. | 进料口A进入的是NaClO溶液,而出料口B输出的则是NaCl溶液 |
16.解释下列物质性质的变化规律时,与共价键的键能无关的是( )
| A. | N2比P4的化学性质稳定 | |
| B. | F2、C12、Br2、I2的沸点逐渐升高 | |
| C. | 金刚石的熔点比晶体硅高 | |
| D. | HF、HCl、HBr、HI的热稳定性依次减弱 |
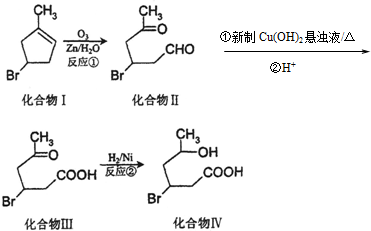
 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$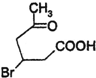 +Cu2O↓+2H2O.
+Cu2O↓+2H2O.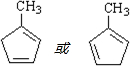 .
. .
.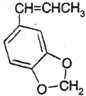 发生类似反应①的反应,得到乙醛和化合物Y,Y的结构简式为
发生类似反应①的反应,得到乙醛和化合物Y,Y的结构简式为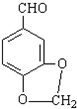 .
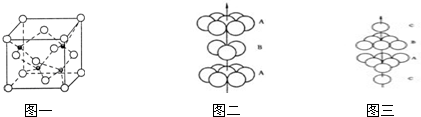
.
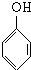 +nHCHO$\stackrel{浓盐酸}{→}$
+nHCHO$\stackrel{浓盐酸}{→}$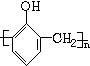 +nH2O.
+nH2O.