��Ŀ����
��ѧ����Դ����������������ʮ�ֹؼ������á�
��1���̲��ں��ġ���ȼ�����Ǹ�ѹ���γɵ��������ļ���ˮ������塣��������ȼ�յ��Ȼ�ѧ����ʽΪ��CH4(g)��2O2(g)��CO2(g)��2H2O(l) ��H����890.3 kJ��mol��
356g����ȼ����(����ʽΪCH4��9H2O)�ͷŵļ���������ȫȼ������Һ̬ˮ���ų�������Ϊ _______ ��
��2��ij��ȼ�ϵ�أ�һ���缫ͨ���������һ�缫ͨ��Һ��ʯ����(��C4H10��ʾ)����صĵ�����Dz�����Y2O3��ZrO2���壬���ڸ����´���O2����
��֪�õ�ظ����ĵ缫��ӦΪ��C4H10��2O2����4e����CO2��H2O����õ�������ĵ缫��ӦʽΪ _______ ����ع���ʱ�������������O2���� _______ ���ƶ���
 ��3����֪һ����̼��ˮ�����ķ�ӦΪ��CO(g)��H2O(g) CO2(g)��H2(g)
��3����֪һ����̼��ˮ�����ķ�ӦΪ��CO(g)��H2O(g) CO2(g)��H2(g)
��T��ʱ����һ������������У�ͨ��һ������CO(g)��H2O(g)��������Ӧ�������¶Ȳ��䣬������Ũ����ʱ��仯���±��� T��ʱ���ʵ�Ũ��(mol/L)�仯
��5��6minʱ�������DZ����¶Ⱥ��������ʱ���ı�ijһ�������õġ���4��5min֮�䣬�ı�������� _______ ����5��6min֮�䣬�ı�������� _______ ��T��ʱ�û� ѧ��Ӧ��ƽ�ⳣ���� _______ ��
����֪420��ʱ���û�ѧ��Ӧ��ƽ�ⳣ��Ϊ9�������Ӧ��ʼʱ��CO��H2O(g)��Ũ�ȶ���0.01 mol��L����CO�ڴ������µ�ת����Ϊ _______ ��
��397��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ12�����жϸ÷�Ӧ�ġ�H _______ 0(�>��������������<��)��
��1���̲��ں��ġ���ȼ�����Ǹ�ѹ���γɵ��������ļ���ˮ������塣��������ȼ�յ��Ȼ�ѧ����ʽΪ��CH4(g)��2O2(g)��CO2(g)��2H2O(l) ��H����890.3 kJ��mol��
356g����ȼ����(����ʽΪCH4��9H2O)�ͷŵļ���������ȫȼ������Һ̬ˮ���ų�������Ϊ _______ ��
��2��ij��ȼ�ϵ�أ�һ���缫ͨ���������һ�缫ͨ��Һ��ʯ����(��C4H10��ʾ)����صĵ�����Dz�����Y2O3��ZrO2���壬���ڸ����´���O2����
��֪�õ�ظ����ĵ缫��ӦΪ��C4H10��2O2����4e����CO2��H2O����õ�������ĵ缫��ӦʽΪ _______ ����ع���ʱ�������������O2���� _______ ���ƶ���
 ��3����֪һ����̼��ˮ�����ķ�ӦΪ��CO(g)��H2O(g) CO2(g)��H2(g)
��3����֪һ����̼��ˮ�����ķ�ӦΪ��CO(g)��H2O(g) CO2(g)��H2(g)��T��ʱ����һ������������У�ͨ��һ������CO(g)��H2O(g)��������Ӧ�������¶Ȳ��䣬������Ũ����ʱ��仯���±��� T��ʱ���ʵ�Ũ��(mol/L)�仯
| ʱ�� / min | CO | H2O(g) | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
����֪420��ʱ���û�ѧ��Ӧ��ƽ�ⳣ��Ϊ9�������Ӧ��ʼʱ��CO��H2O(g)��Ũ�ȶ���0.01 mol��L����CO�ڴ������µ�ת����Ϊ _______ ��
��397��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ12�����жϸ÷�Ӧ�ġ�H _______ 0(�>��������������<��)��
��1��1780.6 kJ ��2��O2��4e����2O2���� ��
��3��������H2Ũ�ȣ�����H2O(g)Ũ�ȣ� 0.5 �� 75�� �� <
��3��������H2Ũ�ȣ�����H2O(g)Ũ�ȣ� 0.5 �� 75�� �� <
��1��356�˿�ȼ����2mol������890.3��2=1780.6��
��2������ȼ�շ���ʽ�Ƶ��ܷ�ӦʽΪ C4H10+ 13/2 O2 �� 4 CO2+ 5 H2O
��ȥ������Ӧʽ C4H10+13O2--26e- 4CO2+5H2O
13/2 O2-��13O2--26e-��=0 �����ã� O2+4e-=O2-
��3����K= ��0.1��0.1��/��0.1��0.2��="0.5" ��
���裺����ʼ��ƽ��CO��Ũ�ȱ仯Ϊx mol��L -1
H2O (g) �� CO (g) H2(g)�� CO2 (g)
H2(g)�� CO2 (g)
��ʼ��0.01 0.01 0 0
�仯��x x x x
ƽ�⣺(0.01��x) (0.01��x) x x
����¶��·�Ӧ��ƽ�ⳣ��k = x2/(0.01��x)2=9�����x =0.0075��ת����Ϊ75%��
��420��ʱ���û�ѧ��Ӧ��ƽ�ⳣ��Ϊ9��397��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ12��ƽ�ⳣ������˵��ƽ�������ƶ���������ƽ�������ƶ�������Ӧ���ȣ���H��0��
��2������ȼ�շ���ʽ�Ƶ��ܷ�ӦʽΪ C4H10+ 13/2 O2 �� 4 CO2+ 5 H2O
��ȥ������Ӧʽ C4H10+13O2--26e- 4CO2+5H2O
13/2 O2-��13O2--26e-��=0 �����ã� O2+4e-=O2-
��3����K= ��0.1��0.1��/��0.1��0.2��="0.5" ��
���裺����ʼ��ƽ��CO��Ũ�ȱ仯Ϊx mol��L -1
H2O (g) �� CO (g)
 H2(g)�� CO2 (g)
H2(g)�� CO2 (g)��ʼ��0.01 0.01 0 0
�仯��x x x x
ƽ�⣺(0.01��x) (0.01��x) x x
����¶��·�Ӧ��ƽ�ⳣ��k = x2/(0.01��x)2=9�����x =0.0075��ת����Ϊ75%��
��420��ʱ���û�ѧ��Ӧ��ƽ�ⳣ��Ϊ9��397��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ12��ƽ�ⳣ������˵��ƽ�������ƶ���������ƽ�������ƶ�������Ӧ���ȣ���H��0��

��ϰ��ϵ�д�
�����Ŀ
 bB(g)
bB(g) 3C��g��+2D(g) ��H��0,��������ڵķ�Ӧ�ﵽ��ѧƽ�⣬A��Ũ��Ϊ2.4mol��L-1��B��Ũ��Ϊ1.8mol��L-1��tmin���������ﵽ��ѧƽ�⣬B��Ũ��Ϊ0.8mol��L-1��������Ŀ������Ϣ�ش���������:
3C��g��+2D(g) ��H��0,��������ڵķ�Ӧ�ﵽ��ѧƽ�⣬A��Ũ��Ϊ2.4mol��L-1��B��Ũ��Ϊ1.8mol��L-1��tmin���������ﵽ��ѧƽ�⣬B��Ũ��Ϊ0.8mol��L-1��������Ŀ������Ϣ�ش���������: pC������+qD������+ Q�������жϣ�������ȷ����
pC������+qD������+ Q�������жϣ�������ȷ���� 
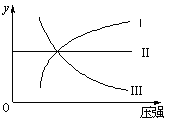
 2NH3(g) ��H��0�����ߢ�
2NH3(g) ��H��0�����ߢ� 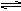 2Z�����ﵽ��ѧƽ��ʱ����Ӧ�������ʵ����������������ʵ�����ȣ���ʱx��ת������( )��
2Z�����ﵽ��ѧƽ��ʱ����Ӧ�������ʵ����������������ʵ�����ȣ���ʱx��ת������( )�� 2AB(g)�ﵽƽ��ı�־��
2AB(g)�ﵽƽ��ı�־��