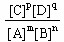题目内容
在500K,相同体积的甲、乙容器,甲容器中充入m g SO2和m g O2,乙容器中充入n g SO2和n g O2 (n>m),则下列叙述错误的是( )
| A.化学反应速率:乙>甲 | B.平衡时O2的浓度:乙>甲 |
| C.SO2的转化率:甲>乙 | D.平衡时SO2的体积分数:甲<乙 |
CD
我们先设计一个丙容器,它与甲保持压强相等,则甲、丙达到平衡时,两者是等效平衡,其中的反应速率、平衡时O2的浓度、SO2的转化率以及平衡时SO2的体积分数均相等;而乙相当于在丙的基础之上,给丙加压,则此时的平衡向正反应方向移动,从而使化学反应速率:乙>甲,平衡时O2的浓度:乙>甲,SO2的转化率:甲<乙,平衡时SO2的体积分数:甲>乙。

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
 2Z(g)。已知X2、Y2、Z的起始浓度分别为0.1mol·L-1、0.3mol·L-1、0.2mol·L-1,当反应在一定条件下达到平衡时各物质浓度可能是( )
2Z(g)。已知X2、Y2、Z的起始浓度分别为0.1mol·L-1、0.3mol·L-1、0.2mol·L-1,当反应在一定条件下达到平衡时各物质浓度可能是( )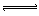 2SO3(气)
2SO3(气) (3)已知一氧化碳与水蒸气的反应为:CO(g)+H2O(g) CO2(g)+H2(g)
(3)已知一氧化碳与水蒸气的反应为:CO(g)+H2O(g) CO2(g)+H2(g) 2SO3(g),根据下列要求填写空白:
2SO3(g),根据下列要求填写空白:
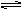 PC(g)达到化学平衡时,缩小密闭容器的体积,发现A的转化率降低,下列关系普遍运用于上述一类反应的是( )
PC(g)达到化学平衡时,缩小密闭容器的体积,发现A的转化率降低,下列关系普遍运用于上述一类反应的是( )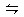 xC(g),达到平衡后,C的体积分数为W% 。若维持容器体积和温度不变,按0.6 mol A、0.3 mol B、1.4 mol C 为起始物质,达到平衡后,C的体积分数也为W% ,则x值为( )
xC(g),达到平衡后,C的体积分数为W% 。若维持容器体积和温度不变,按0.6 mol A、0.3 mol B、1.4 mol C 为起始物质,达到平衡后,C的体积分数也为W% ,则x值为( )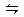 I2(g)+H2(g),增大压强可使平衡体系颜色变深
I2(g)+H2(g),增大压强可使平衡体系颜色变深 p C(g)+q D(g)的平衡常数为K,下列说法不正确的是 ( )
p C(g)+q D(g)的平衡常数为K,下列说法不正确的是 ( )