题目内容
【题目】(1)硅酸盐可以改写成氧化物的形式,将下列硅酸盐改写成氧化物的形式:
①镁橄榄石(Mg2SiO4):____。
②高岭石[Al2(Si2O5)(OH)4]:____。
(2)写出下列反应的方程式:
①漂白粉露置于空气中较长时间后失效的化学方程式: _________________________。
②Cl2通入NaOH溶液中,发生反应的离子方程式:________________________。
③NO2与水反应的化学方程式为___________,该反应中氧化剂与还原剂的物质的量之比为_____________.
【答案】2MgOSiO2 Al2O32SiO22H2O Ca(ClO)2+CO2+H2O=CaCO)3+2HClO、2HClO![]() 2HCl+O2↑ Cl2+2OH-=Cl-+ClO-+H2O 3NO2+H2O=2HNO3+NO 1:2
2HCl+O2↑ Cl2+2OH-=Cl-+ClO-+H2O 3NO2+H2O=2HNO3+NO 1:2
【解析】
(1)硅酸盐由盐的书写改写为氧化物的一般形式:碱性氧化物、两性氧化物、酸性氧化物、水;
(2)漂白粉露置于空气中首先生成次氯酸,次氯酸见光分解后失效;氯气与NaOH反应生成氯化钠、次氯酸钠和水;NO2与水反应生成NO和硝酸,氧化剂与还原剂的物质的量之比等于还原产物NO与氧化产物HNO3的物质的量之比。
(1)硅酸盐由盐的书写改写为氧化物的一般形式:碱性氧化物、两性氧化物、酸性氧化物、水,注意各种元素化合价不变;
①橄榄石(Mg2SiO4)改写成氧化物形式为:2MgOSiO2;故答案为:2MgOSiO2;
②高岭石[Al2(Si2O5)(OH)4]改写为氧化物形式为:Al2O32SiO22H2O;故答案为:Al2O32SiO22H2O;
(2)①漂白粉露置于空气中失效的化学反应方程式为Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO,2HClO![]() 2HCl+O2↑,故答案为:Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO、2HClO
2HCl+O2↑,故答案为:Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO、2HClO![]() 2HCl+O2↑;
2HCl+O2↑;
②氯气与氢氧化钠反应生成氯化钠、次氯酸与水,反应离子方程式Cl2+2OH-=ClO-+Cl-+H2O,
故答案为:Cl2+2OH-=ClO-+Cl-+H2O;
③NO2与水反应生成NO和硝酸,化学方程式为3NO2+H2O=2HNO3+NO,还原产物NO与氧化产物HNO3的物质的量之比为1:2,因此氧化剂与还原剂的物质的量之比为1:2,故答案为:3NO2+H2O=2HNO3+NO;1:2。

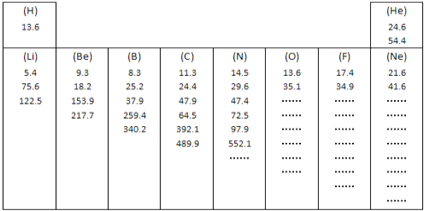
【题目】下图是元素周期表的一部分:
① | |||||||||||||||||
④ | ⑤ | ⑥ | |||||||||||||||
② | ③ | ⑦ | ⑧ | ||||||||||||||
Fe | |||||||||||||||||
Ⅰ.用化学用语回答下列问题:
(1)①、②、⑥形成的化合物中存在的化学键类型有________。
(2)④、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是_______。
(3)写出②的离子结构示意图为__________。
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。Y的水溶液与洁厕灵混合使用会产生一种有毒气体,该反应的离子方程式为_______。
Ⅱ.A、B、C、D都是中学化学中常见的物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。根据题意回答下列问题:
![]()
(1)若A是一种金属单质,C是淡黄色固体,写出C的一种用途_____;
(2)若A、B、C均为化合物且含有同一种金属元素,D是会造成温室效应的一种气体,请写出D的电子式_____,A和C反应的离子方程式 ___。
(3)若D是一种常见的过渡金属单质,原子核内有26个质子,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,检验此C溶液中金属离子的方法是________;又知在酸性溶液中该金属离子能被双氧水氧化,写出该反应的离子方程式_________。