题目内容
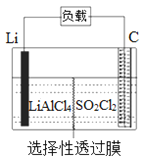
【题目】某同学设计一个燃料电池(如下图所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
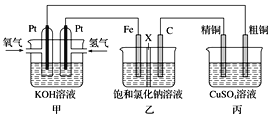
(1)通入氢气的电极为________ (填正极或负极),该电极反应式为________。
(2)石墨电极为________ (填阳极或阴极),乙中总反应化学方程式为________;如果把铁电极和石墨电极交换,乙溶液左侧出现的现象是_________。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将__________(填“增大”“减小”或“不变”)。
(4)若甲中消耗0.01mol O2,丙中精铜增重_________克。
【答案】负极 H2-2e-+2OH-=2H2O 阳极 2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑ 溶液中有气泡逸出;起初产生白色沉淀,然后白色沉淀迅速转化为灰绿色,最后转化为红褐色。 减小 1.28g
2NaOH+H2↑+Cl2↑ 溶液中有气泡逸出;起初产生白色沉淀,然后白色沉淀迅速转化为灰绿色,最后转化为红褐色。 减小 1.28g
【解析】
从图中可以看出,甲池为原电池(作电源),乙池为电解池,丙池为铜的电解精炼。甲池中,通氢气的电极为负极,通氧气的电极为正极;乙池中,Fe电极为阴极,C电极为阳极;丙池中,精铜为阴极,粗铜为阳极。
(1)通入氢气的电极为负极,负极的电极反应式为:H2-2e-+2OH-=2H2O,答案为负极;H2-2e-+2OH-=2H2O;
(2)石墨电极为阳极,乙中总反应化学方程式为:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;如果把铁电极和石墨电极交换,乙溶液右侧发生的反应为Fe-2e-=Fe2+,通过阳离子交换膜进入乙池的左侧,在乙池的左侧,发生的反应为2H2O+2e-=2OH-+H2↑,Fe2++2OH-=Fe(OH)2↓,4Fe(OH)2+O2+2H2O=4Fe(OH)3,所以乙池左侧出现的现象是:溶液中有气泡逸出;起初产生白色沉淀,然后白色沉淀迅速转化为灰绿色,最后转化为红褐色,答案为阳极;2NaCl+2H2O
2NaOH+H2↑+Cl2↑;如果把铁电极和石墨电极交换,乙溶液右侧发生的反应为Fe-2e-=Fe2+,通过阳离子交换膜进入乙池的左侧,在乙池的左侧,发生的反应为2H2O+2e-=2OH-+H2↑,Fe2++2OH-=Fe(OH)2↓,4Fe(OH)2+O2+2H2O=4Fe(OH)3,所以乙池左侧出现的现象是:溶液中有气泡逸出;起初产生白色沉淀,然后白色沉淀迅速转化为灰绿色,最后转化为红褐色,答案为阳极;2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;溶液中有气泡逸出;起初产生白色沉淀,然后白色沉淀迅速转化为灰绿色,最后转化为红褐色;
2NaOH+H2↑+Cl2↑;溶液中有气泡逸出;起初产生白色沉淀,然后白色沉淀迅速转化为灰绿色,最后转化为红褐色;
(3)如果粗铜中含有锌、银等杂质,丙装置中发生的反应为:阳极:Zn-2e-=Zn2+,Cu-2e-=Cu2+;阴极:Cu2++2e-=Cu,因为线路中通过电子的物质的量相等,所以随着电解反应的进行,溶液中Cu2+不断减小,答案为减小;
(4)可通过电子守恒建立以下关系式
O2——4e-——2Cu
0.01mol 0.02mol
![]() ,
,
答案为1.28g。

 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案