题目内容
【题目】如表是元素周期表的一部分,其中每个数字编号代表一种短周期元素。

请按要求回答下列问题:
(1)元素②的元素名称是____。
(2)元素⑤处于周期表中第____周期第___族。
(3)①⑦七种元素中原子半径最大的是___(填元素符号)。②③④三种元素的最简单氢化物中最稳定的是____(填化学式)。
(4)元素③和元素⑦的氢化物均极易溶于水,且二者能反应产生大量白烟,写出该白色物质发生分解的化学方程式______。
(5)元素⑥的最高价氧化物对应的水化物是一种____性氢氧化物,该物质与元素⑦的最高价氧化物对应水化物反应的离子方程式为_____。
【答案】碳 三 IA Na H2O ![]() 两
两 ![]()
【解析】
根据元素周期表推断各种元素种类;根据元素周期律分析各元素的性质和结构;
根据元素在周期表中的位置分析可知,①是H,②是C,③是N,④是O,⑤是Na,⑥是Al,⑦是Cl,
(1)元素②的元素是碳元素;
(2)元素⑤是Na元素,处于周期表中第三周期第IA族;
(3)同周期元素从左到右,原子半径逐渐减小,同主族元素从上到下,原子半径逐渐增大,则①⑦七种元素中原子半径最大的是第三周期最左边的Na;同周期元素从左到右,非金属性逐渐增强,②③④三种元素的非金属性,O>N>C,非金属性越强,气态氢化物就越稳定,则其最简单氢化物中最稳定的是H2O;
(4)元素③是N和元素⑦是Cl,它们的氢化物分别为NH3和HCl,它们反应生成的是NH4Cl,NH4Cl受热分解生成HCl和NH3,方程式为:NH4Cl![]() NH3↑+HCl↑;
NH3↑+HCl↑;
(5)元素⑥是Al,它的最高价氧化物对应的水化物是Al(OH)3,是一种两性氢氧化物,元素⑦是Cl,它的最高价氧化物的水化物为HClO4,Al(OH)3和HClO4反应生成Al(ClO4)3和水,离子方程式为Al(OH)3 + 3H+ = Al3+ + 3H2O;

 阅读快车系列答案
阅读快车系列答案【题目】已知化学反应①:Fe(s)+CO2(g)![]() FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)![]() FeO(s)+H2(g),其平衡常数为K2,化学反应③CO2(g)+H2(g)
FeO(s)+H2(g),其平衡常数为K2,化学反应③CO2(g)+H2(g)![]() H2O(g)+CO(g),其平衡常数为K3,在温度为973K和1173K情况下,K1、K2的值分别如下:
H2O(g)+CO(g),其平衡常数为K3,在温度为973K和1173K情况下,K1、K2的值分别如下:
温度 | K1 | K2 |
973 K | 1.47 | 2.38 |
1173 K | 2.15 | 1.67 |
请填空:
(1)通过表格中的数值可以推断:反应①是____(填“吸热”或“放热”)反应。
(2)根据反应①与②可推导出K1、K2与K3之间的关系式_____,据此关系式及上表数据,也能推断出反应③是____(填“吸热”或“放热”)反应。
(3)要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有____。
A.缩小反应容器的容积
B.扩大反应容器的容积
C.升高温度
D.使用合适的催化剂
E.设法减小平衡体系中CO的浓度
(4)图甲、图乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:
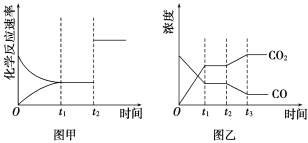
①图甲t2时刻改变的条件是___。②图乙t2时刻改变的条件是__。
【题目】工业生产中常用炼锌废渣(含有ZnO、FeO、Fe2O3、CuO等杂质)来提取氧化锌和金属铜等,其主要工艺流程如图所示:

有关氢氧化物开始沉淀和沉淀完全的pH见下表
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 5.4 | 6.5 |
沉淀完全的pH | 3.7 | 9.7 | 6.7 | 8.0 |
(1)为提高浸出速率,除适当增加硫酸浓度外,还可采取的措施有(写出两条) ______
(2)试剂A是 ______ (填化学式).
(3)调节酸浸液的pH的范围是 ______.
(4)滤液甲与试剂B发生置换反应,则试剂B是 ______ (填化学式).
(5)在实验室进行焙烧时,盛放沉淀丙的仪器名称是 ______ .