题目内容
11.用0.1mol/L的FeSO4溶液100mL,恰好将2×10-3mol的XO4-还原,则元素X在还原产物中的化合价是( )| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
分析 FeSO4恰好将XO4-还原,反应中Fe2+变成Fe3+,则X的化合价降低,利用电子守恒计算解答.
解答 解:(FeSO4)=0.1mol/L×0.1L=0.01mol,恰好将XO4-还原,反应中Fe2+变成Fe3+,失去0.01mol电子,
n(XO4-)=2×10-3mol,假设还原后的化合价为n,
由电子守恒可知,
0.01mol×(3-2)=2×10-3mol×(7-n),
n=2,
故选B.
点评 本题考查氧化还原反应的计算,侧重于学生的分析、计算能力的考查,明确氧化还原反应中元素的化合价升降及电子守恒是解答本题的关键,题目难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
1.下列水溶液中电离方程式,书写正确的是( )
| A. | AlCl3═Al3++Cl3- | B. | NaHSO4═Na++H++SO42- | ||
| C. | Mg(NO3)2═Mg+2+2NO3- | D. | NaHCO3═Na++H++CO32- |
6.通常情况下,下列物质中,不能使酸性高锰酸钾溶液褪色,但能使溴水层颜色变浅的是( )
| A. | 亚硫酸 | B. | 辛烷 | C. | 碘化钾溶液 | D. | 四氯化碳 |
6.许多马路两旁的树干都均匀地涂抹了石灰水.下列有关说法正确的是( )
| A. | 饱和石灰水加入生石灰,若温度不变,则溶液中Ca2+的物质的量不变 | |
| B. | 饱和石灰水加入生石灰,若温度不变,则pH不变 | |
| C. | 升高饱和石灰水的温度时,Ca(OH)2的溶度积常数Ksp不变 | |
| D. | 石灰水显碱性,能使蛋白质变性,所以有防治树木害虫病的作用 |
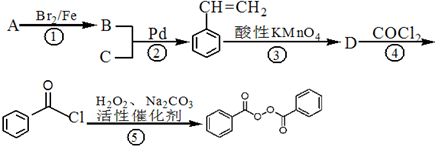
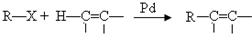
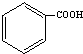 ;
;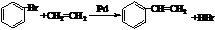 ;
; ),在一定条件下能发生银镜反应,且1molE最多可消耗4mol NaOH
),在一定条件下能发生银镜反应,且1molE最多可消耗4mol NaOH 的流程,无机物任选,注明反应条件.
的流程,无机物任选,注明反应条件.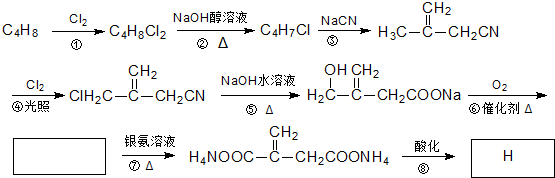
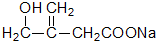 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2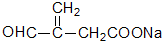 +2H2O;其反应类型是氧化反应;
+2H2O;其反应类型是氧化反应;