题目内容
19.一定条件下,有反应X(g)+2Y(g)?nZ(g),△H=QkJ/mol(n为正整数),在体积为2L的密闭容器中,充入1mol X和1mol Y进行反应,2min钟后反应达到平衡,此时平衡混合物中X为0.8mol,则以Y浓度变化表示的反应速率为0.1mol/(L•min)分析 根据在体积为2L的密闭容器中,充入1mol X和1mol Y进行反应,2min钟后反应达到平衡,此时平衡混合物中X为0.8mol计算X的反应速率再结合速率之比等于系数之比计算以Y浓度变化表示的反应速率.
解答 解:因为在体积为2L的密闭容器中,充入1mol X和1mol Y进行反应,2min钟后反应达到平衡,此时平衡混合物中X为0.8mol,则X的反应速率=$\frac{\frac{1-0.8}{2}}{2}$=0.05mol/(L•min),又速率之比等于系数之比,所以以Y浓度变化表示的反应速率为0.05mol/(L•min)×2=0.1mol/(L•min),故答案为:0.1.
点评 本题考查化学反应速率的计算,难度不大,利用速率之比等于系数之比即可.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
9.298K时,0.5molN2(g)与适量H2(g)转化成NH3(g)放出46.1kJ的热量,则表示该反应的热化学方程式正确的是( )
| A. | N2(g)+3H2(g)═2NH3(g)△H(298K)=+92.2kJ•mol-1 | |
| B. | N2(g)+3H2(g)═2NH3(g)△H(298K)=-92.2kJ•mol-1 | |
| C. | N2(g)+3H2(g)═2NH3(g)△H(298K)=+46.1kJ•mol-1 | |
| D. | N2(g)+3H2(g)═2NH3(g)△H(298K)=-46.1kJ•mol-1 |
10.某固体物质只含有钠和氧两种元素,将它放在足量的水中产生两种气体,这两种气体又可以在一定条件下反应生成水.则原固体物质的组成是( )
| A. | Na2O2与Na2O | B. | Na和NaOH量 | C. | Na和Na2O | D. | Na2O2和Na |
7.漂白粉的有效成分是( )
| A. | CaCl2 和Ca(ClO)2 | B. | Ca(ClO)2 | C. | CaCl2 | D. | CaCO3 |
14.1mol•L-1的NaCl溶液表示( )
| A. | 溶液中含有1 mol NaCl | B. | 1 mol NaCl溶于1 L水中 | ||
| C. | 58.5 g NaCl溶于941.5 g水中 | D. | 1 L溶液中含有NaCl 58.5 g |
4.向50g FeCl3溶液中放入一小块Na,待反应完全后,过滤,得到仍有棕黄色的溶液45.9g,则投入的Na的质量为( )
| A. | 4.6g | B. | 4.1g | C. | 6.9g | D. | 9.2g |
11.用0.1mol/L的FeSO4溶液100mL,恰好将2×10-3mol的XO4-还原,则元素X在还原产物中的化合价是( )
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
 A、B、C、D均是由短周期元素形成的四种气体单质,E、F均为气体,且F为红棕色.有关的转化关系如图所示(反应条件均已略去):
A、B、C、D均是由短周期元素形成的四种气体单质,E、F均为气体,且F为红棕色.有关的转化关系如图所示(反应条件均已略去):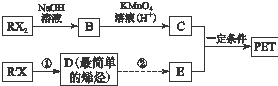 PET是聚酯类合成材料,以卤代烃为原料合成PET的线路如图(反应中部分无机反应物及产物已省略).已知RX2(R、R′代表烃基,X代表卤素原子)是芳香族化合物,相对分子质量为175,其中X元素的质量分数为40.6%.
PET是聚酯类合成材料,以卤代烃为原料合成PET的线路如图(反应中部分无机反应物及产物已省略).已知RX2(R、R′代表烃基,X代表卤素原子)是芳香族化合物,相对分子质量为175,其中X元素的质量分数为40.6%. .
.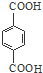 +nHOCH2CH2OH$\stackrel{一定条件下}{→}$
+nHOCH2CH2OH$\stackrel{一定条件下}{→}$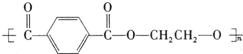 +2nH2O.
+2nH2O.