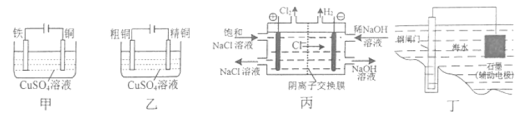
��Ŀ����
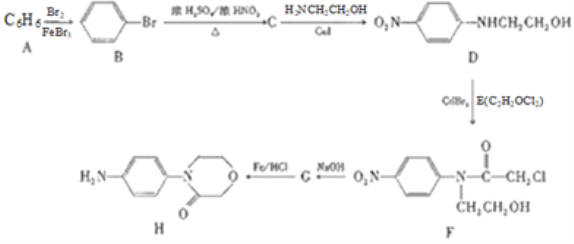
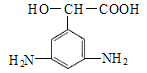
����Ŀ��H�Ǻϳ�Ԥ������Ѫ˨�γ�(![]() )��ԭ��ҩ����ɳ���м��壬��ϳ�·����ͼ��
)��ԭ��ҩ����ɳ���м��壬��ϳ�·����ͼ��
��֪��
(1)A�Ļ�ѧ����Ϊ_________________��C�к��й����ŵ�����Ϊ__________________��
(2)C��D�ķ�Ӧ����Ϊ__________________��
(3)G�Ľṹ��ʽΪ______________________��
(4)D��F�Ļ�ѧ����ʽΪ__________________________________________________��
(5)��������������D��ͬ���칹����_______________��(�����������칹)�����к˴Ź���������6����ҷ����֮��Ϊ4:2:1:1:1:1�Ľṹ��ʽΪ____________________(дһ��)��
�ٱ�������3��ȡ����������������ֱ�Ӻͱ����������ۿ��Ժ�![]() ��Һ��Ӧ����
��Һ��Ӧ����![]() �������������Ʒ�Ӧ����
�������������Ʒ�Ӧ����![]() ��
��
(6)��֪��![]() ����CΪԭ�Ϻϳ�
����CΪԭ�Ϻϳ�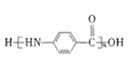 �ĺϳ�·��Ϊ____________________________________________(�����Լ���ѡ)��
�ĺϳ�·��Ϊ____________________________________________(�����Լ���ѡ)��
���𰸡��� ��ԭ�ӡ����� ȡ����Ӧ 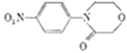
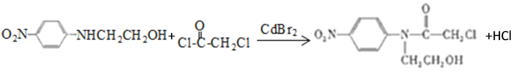 6
6 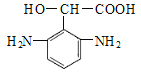 ��
��
��������
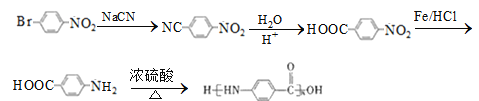
������ͼ��֪��AΪ�� ![]() �����廯���Ĵ������±���Һ�巢��ȡ����Ӧ����B�屽����Ũ������������屽��Ũ���ᷢ��������Ӧ����C����D�Ľṹ��ʽ��֪��C�Ľṹ��ʽΪ
�����廯���Ĵ������±���Һ�巢��ȡ����Ӧ����B�屽����Ũ������������屽��Ũ���ᷢ��������Ӧ����C����D�Ľṹ��ʽ��֪��C�Ľṹ��ʽΪ![]() ��C��H2NCH2CH2OH����ȡ����Ӧ����D��D��E����ȡ����Ӧ����F����D��F�Ľṹ��ʽ�����E�ķ���ʽ��֪��E�Ľṹ��ʽΪ
��C��H2NCH2CH2OH����ȡ����Ӧ����D��D��E����ȡ����Ӧ����F����D��F�Ľṹ��ʽ�����E�ķ���ʽ��֪��E�Ľṹ��ʽΪ![]() ��������֪��Ϣ��Ӧ֪��G������ԭ��Ӧ����H����GΪ
��������֪��Ϣ��Ӧ֪��G������ԭ��Ӧ����H����GΪ ��F��NaOH�����·�Ӧ����G���ݴ˷������
��F��NaOH�����·�Ӧ����G���ݴ˷������
(1)A�Ļ�ѧ����Ϊ����CΪ![]() �����й����ŵ�����Ϊ��ԭ�ӡ�������
�����й����ŵ�����Ϊ��ԭ�ӡ�������
(2)CΪ![]() ��C��H2NCH2CH2OH��Ӧʱ��-NHCH2CH2OHȡ����C�е���ԭ������D����C��H2NCH2CH2OH����ȡ����Ӧ����D��
��C��H2NCH2CH2OH��Ӧʱ��-NHCH2CH2OHȡ����C�е���ԭ������D����C��H2NCH2CH2OH����ȡ����Ӧ����D��
(3)G�Ľṹ��ʽΪ ��
��
(4)D��E����ȡ����Ӧ����F����D��F�Ļ�ѧ����ʽΪ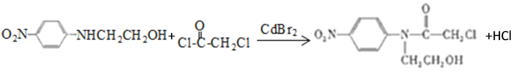 ��
��
(5)��������������D��ͬ���칹�壬�ٱ�������3��ȡ����������������ֱ�Ӻͱ����������ۿ��Ժ�![]() ��Һ��Ӧ��˵����һ���Ȼ�����
��Һ��Ӧ��˵����һ���Ȼ�����![]() �������������Ʒ�Ӧ����
�������������Ʒ�Ӧ����![]() ��˵������һ���ǻ�������һ��ȡ����Ϊ
��˵������һ���ǻ�������һ��ȡ����Ϊ![]() ������������λ����λʱ��
������������λ����λʱ��![]() ��2��ȡ����ʽ������������λ�ڶ�λʱ��
��2��ȡ����ʽ������������λ�ڶ�λʱ��![]() ��1��ȡ����ʽ������������λ�ڼ�λʱ��
��1��ȡ����ʽ������������λ�ڼ�λʱ��![]() ��3��ȡ����ʽ�������������ͬ���칹�干6�֣����к˴Ź���������6����ҷ������Ϊ4:2:1:1:1:1�Ľṹ��ʽΪ
��3��ȡ����ʽ�������������ͬ���칹�干6�֣����к˴Ź���������6����ҷ������Ϊ4:2:1:1:1:1�Ľṹ��ʽΪ ��
�� ��
��
(6)������֪��Ϣ��Ӧ��֪��![]() ��NaCN��Ӧ����
��NaCN��Ӧ����![]() ��
��![]() �����������·�Ӧ����
�����������·�Ӧ����![]() ��
��![]() ������ԭ��Ӧ����
������ԭ��Ӧ����![]() ��
��![]() �ٷ������۷�Ӧ����
�ٷ������۷�Ӧ����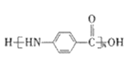 ���ʺϳ�·��Ϊ��
���ʺϳ�·��Ϊ�� ��
��

 �������Ӳ�ϵ�д�
�������Ӳ�ϵ�д� ���ɿ��õ�Ԫ����AB��ϵ�д�
���ɿ��õ�Ԫ����AB��ϵ�д�����Ŀ���Ȼ���ͭ(CuCl)�㷺Ӧ����ұ�𡢵�ơ�ҽҩ����ҵ��ijͬѧ�Ժ�ͭ����(��Ҫ�ɷ��� CuO��MgO��MnO��SiO2������������)Ϊ��Ҫԭ���Ʊ�CuCl����Ҫ�������£�
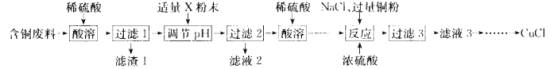
��֪����CuCl������ˮ���Ҵ� ���ڳ�ʪ�Ŀ������ױ�������
����ˮ��Һ�д���ƽ�� ��CuCl(��ɫ)+2Cl-![]() [CuCl3]2-(ɫ����Һ)��
[CuCl3]2-(ɫ����Һ)��
�����ֽ����������↑ʼ��������ȫ������pH���±���
�������� | ��ʼ������ pH | ��ȫ������ pH |
Mg(OH)2 | 8. 4 | 10. 8 |
Cu(OH)2 | 4.2 | 6. 7 |
Mn(OH)2 | 7. 8 | 8. 8 |
�ʴ��������⣺
(1)����1 ����Ҫ�ɷ��� _________________(д��ѧʽ����ͬ)��
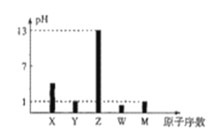
(2)����pH�����÷�ĩ״�Լ� X ��_____________��pH�ĵ��ڷ���Ϊ____________��
(3)����Ӧ������ Cu2+ +Cu+6Cl-=2[CuCl3]2-����������ȫ��Ӧ��������_______________��
(4)������Һ3�� �Ӵ�����ˮ�����˿ɵ� CuCl�����ó����������Ҵ�ϴ�ӣ����ڵ����¸����ԭ����___________��
(5)��Ʒ���ȵIJⶨ���������£���ȡmg����������ƿ�У�����ֱ�� 4 ~ 5 mm ������������������ 10 mL FeCl3��Һ��ҡ������Ʒȫ���ܽ��(CuCl+FeCl3=CuCl2+FeCl2)���ټ���50 mL��ˮ��2���ڷ�����ָʾ����������c mol L-1 ���������[Ce(SO4)2]����Һ�ζ�(Fe2++Ce4+=Fe3++Ce3+)'�����յ�ʱ����������������ҺV mL��
����ƿ�м��벣�����������____________________��
����Ʒ�� CuCl ����������Ϊ_____(�г�����ʽ���� , �ú�(c��m��V�Ĵ���ʽ��ʾ)��
����Ŀ���±���Ԫ�����ڱ���һ���֣���Ա��еĢ١�����Ԫ�أ����û�ѧ����ش��������⣺
�� ���� | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | �� | |||
4 | �� | �� |
��1���ڢۡ���Ԫ���У�ԭ�Ӱ뾶������__________����Ԫ�ط��ţ���
��2����Ԫ�ص�����������Ӧ��ˮ���������⻯����������M��M�к��еĻ�ѧ��������__________________��
��3��д��Ԫ�آٺ͢�ĵ����ڼ��������·�Ӧ���ɵĻ�����ĵ���ʽ��_________��
��4
��5���١�����Ԫ������������Ӧ��ˮ������������ǿ����_____________�������ʻ�ѧʽ���������Ե�����������_________�������ʻ�ѧʽ��,�û�������NaOH��Һ��Ӧ�����ӷ���ʽΪ___________��
��6���õ���ʽ��ʾԪ�آ�����γɻ�����Ĺ���_____________________________��